1973年,白细胞介素6 (Interleukin 6, IL-6)被鉴定为T细胞分泌的可溶性因子,对B细胞产生抗体至关重要。自近50年前被发现以来,IL-6通路已经成为参与健康免疫调节和许多疾病免疫失调的关键途径。在经典途径中,IL-6与其膜结合受体mIL-6R、可溶性受体sIL-6R结合后,与膜蛋白gp130结合形成IL-6-IL-6R-gp130六聚体,触发下游信号转导和基因表达。在反向途径中,IL-6-sIL-6R复合物与gp130结合,启动细胞内信号转导。下一步,JAK-STAT、RAS-RAF等通路被激活,促进细胞增殖、分化、氧化应激和免疫调节。经典的IL-6信号局限于表达IL-6R的细胞(巨噬细胞、中性粒细胞、T细胞等)。但当IL-6水平升高时,由于gp130的普遍存在,该信号被广泛表达。
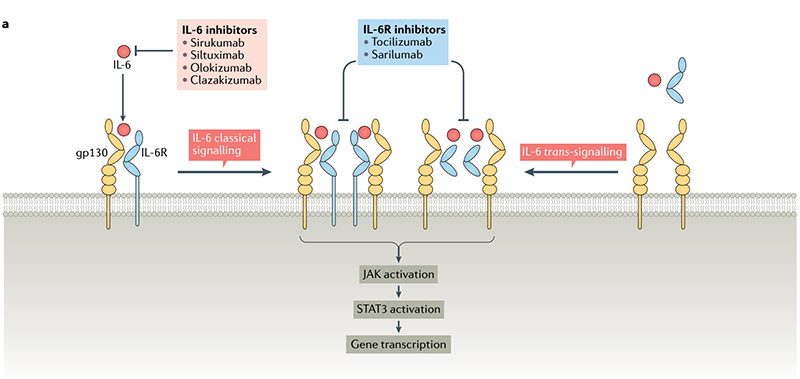
IL-6细胞信号通路
在疾病方面,IL-6可具有局部炎症和全身炎症影响。IL-6与各种疾病的发病机制有关,包括类风湿性关节炎(RA)、系统性幼年特发性关节炎(sJIA)、Castleman病、巨细胞动脉炎(GCA)、大动脉炎、细胞因子释放综合征(CRS)等。IL-6在免疫系统和炎症系统的功能障碍中具有多种作用,anti-IL-6治疗可缓解发热、疲劳、疼痛、关节破坏、贫血等多种症状。

IL-6在免疫系统和炎症系统的功能障碍中具有多种作用
当研究团队发现IL-6信号转导通过一个IL-6, IL-6R和糖蛋白gp130(Glycoprotein 130)六聚体高亲和力复合物介导时,传统的寻找小分子抑制剂的方法具有挑战性。因此,靶向IL-6或IL-6R,阻断IL-6与IL-6R的结合,从而抑制IL-6通路信号转导,这种IL-6通路抑制剂作为多种疾病的潜在治疗手段开启了新历程。起初,研究人员决定以IL-6R为靶点而不是IL-6本身,考虑到受体浓度比IL-6浓度在患者间的可变性更小,这可能简化了剂量和方案的选择。
Tocilizumab(托珠单抗)是首个靶向IL-6R人源化抗体,通过阻止IL-6与IL-6R结合来抑制IL-6信号转导,已获批的多个适应症包括:类风湿性关节炎、多关节型幼年特发性关节炎(pJIA)、全身型幼年特发性关节炎(sJIA)、巨细胞动脉炎(GCA)、细胞因子释放综合征(CRS)、Castleman病、大动脉炎。Tocilizumab包括静脉(IV)制剂和皮下(SC)制剂,在不同国家和地区的具体适应症有所差异。在中国,其IV制剂已被批准用于治疗RA、sJIA、CRS。2021年3月,美国FDA批准Tocilizumab一个新的适应症:用于延缓系统性硬化症相关间质性肺病(SSc-ILD)成人患者肺功能下降的速度。
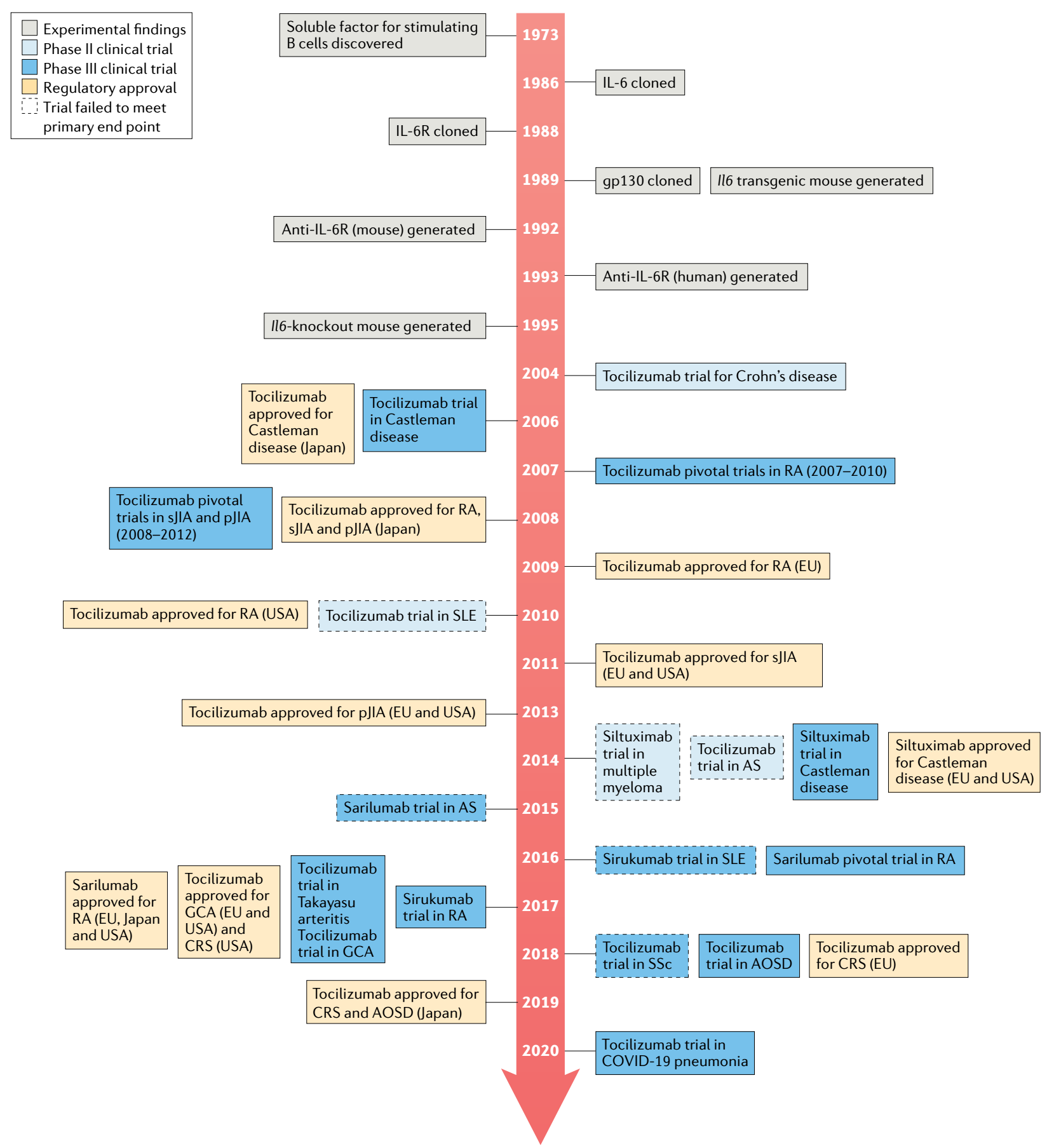
IL-6和IL-6R靶向药物进展
Tocilizumab分别在2017年和2018年获FDA和EMA批准用于治疗严重或危及生命的CAR-T细胞治疗诱导的成人和儿童CRS(使用CD19 CAR-T细胞治疗的患者中,约70%会发展为CRS。CRS可导致头痛、发热、寒战、严重恶心、呕吐、腹泻、肌肉骨骼疼痛、呼吸困难、低血压和心动过速,严重者可致命)。该适应症批准是基于一项回顾性分析数据,该数据显示在前瞻性临床试验中,Tocilizumab治疗对CAR-T细胞治疗后发生CRS的患者的疗效。
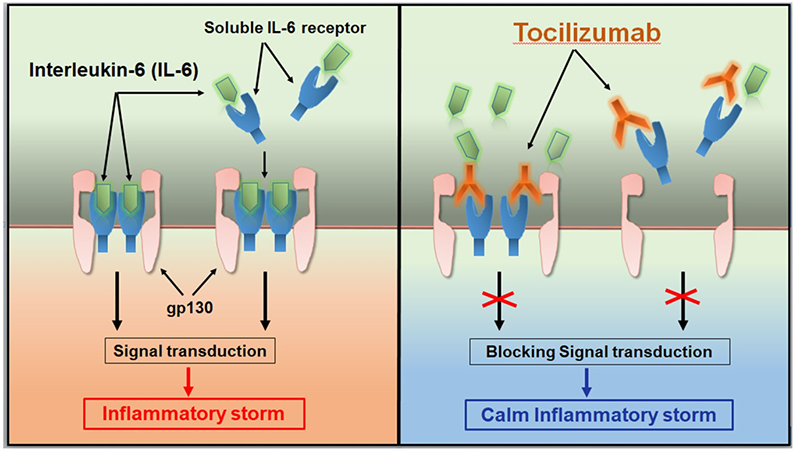
Tocilizumab平息炎症风暴
Tocilizumab这种IL-6R抗体的治疗效益也造就了几种靶向IL-6抗体如sirukumab/西鲁库单抗、olokizumab/奥洛组单抗和clazakizumab/克拉扎珠单抗的开发研究,然而,适应症不尽相同。
以往的回顾性研究认为,新冠肺炎疫情的病情进展可能是由于CRS,IL-6在重度COVID-19患者中的潜在作用被揭示。IL-6和其他促炎细胞因子(如IL-1、IL-8、IL-12)水平的急剧升高在COVID-19患者健康状况恶化中发挥了关键作用。COVID-19感染危重患者IL-6水平升高,而IL-6分泌量高的病原性T细胞和炎性单核细胞可大量进入肺循环,引发炎症风暴,可能导致重症肺炎发展为急性呼吸窘迫综合征,引起免疫功能紊乱最终导致多系统器官衰竭,甚至高死亡率。可以说,IL-6浓度的升高构成了更大规模的细胞因子风暴,从而加重了疾病的后果。因此,IL-6可作为COVID-19危重病例的潜在治疗靶点。
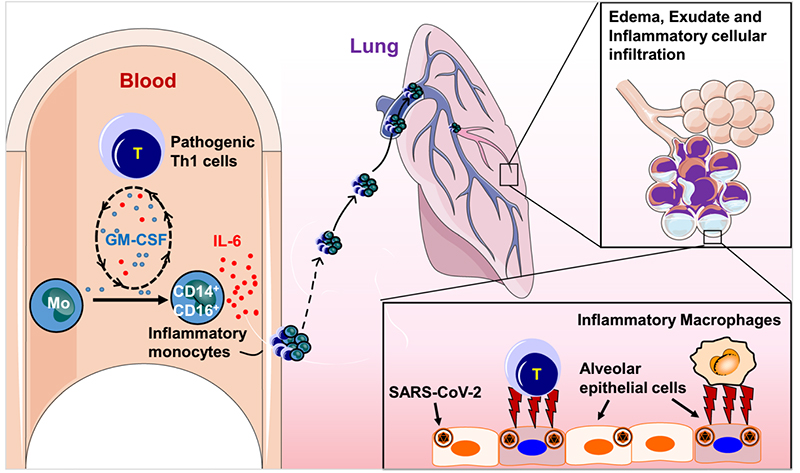
IL-6在COVID-19重症患者疾病进展中的关键作用
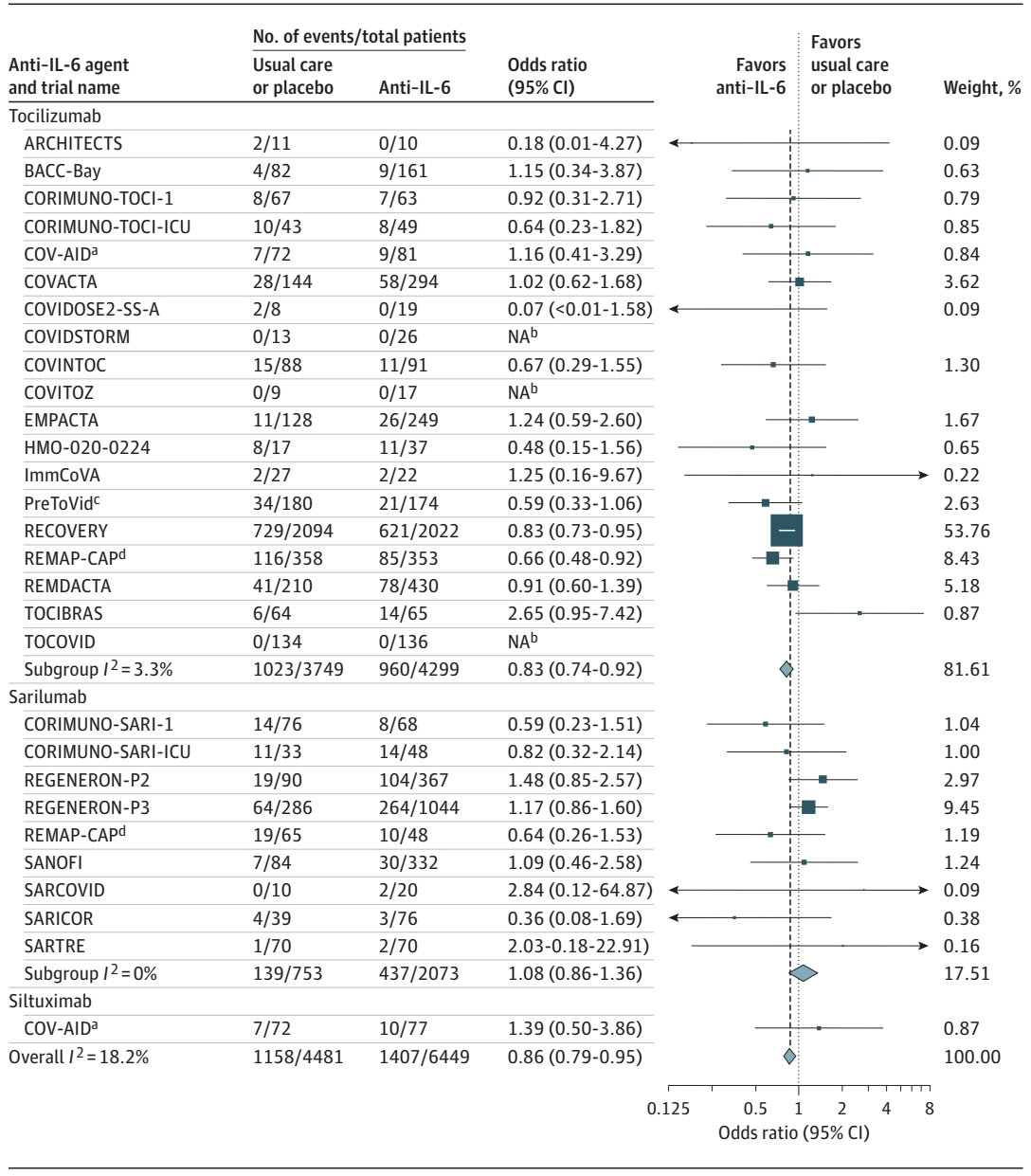
世界卫生组织COVID-19疗法快速证据评估(REACT)工作组,为研究IL-6拮抗剂与在COVID-19住院患者死亡率之间的关系,通过ClinicalTrials.gov,欧盟临床试验登记册和世界卫生组织,国际临床试验注册平台系统检索到72个潜在的合格试验(2020年10月7日至2021年1月11日),其中27个(37.5%)符合研究选择标准。符合条件的COVID-19住院患者被随机分为两组,一组使用IL-6拮抗剂,另一组既不使用IL-6拮抗剂,也不使用除皮质类固醇外的任何其他免疫调节剂。结果共10930例患者(中位年龄61岁)参与了此次27项试验。主要指标是随机分组后28天的全因死亡率。
到了第28天,6449例随机接受IL-6拮抗剂患者中有1407例死亡,4481名随机接受常规治疗或安慰剂治疗的患者中1158例死亡(总体OR, 0.86 [95% CI, 0.79-0.95],P =0.003)。这相当于IL-6拮抗剂的绝对死亡风险为22%,而常规护理或安慰剂的假定死亡风险为25%。相应的汇总ORs为0.83 (95% CI, 0.74-0.92;P < 0.001)和1.08 (95% CI, 0.86-1.36;P = 0.52)。在接受皮质类固醇治疗的患者中,与常规治疗或安慰剂相比,tocilizumab和sarilumab的死亡率相关性总ORs分别为0.77 (95% CI, 0.68-0.87)和0.92 (95% CI, 0.61-1.38)。
在这项针对COVID-19住院患者的临床试验的前瞻性荟萃分析中,与常规治疗或安慰剂相比,IL-6拮抗剂的使用与降低28天全因死亡率有关。
IL-6拮抗剂及常规护理或安慰剂与28天全因死亡率的关系
靶向IL-6通路开启了各种风湿性疾病的创新治疗方法,新发现的证据表明,IL-6的失调导致多种疾病状态,包括各种类型的癌症发展、进展和转移,IL-6水平升高与癌症和其他疾病的高风险有关,如胰岛素抵抗,哮喘,冠心病,晚期癌症,也可以作为癌症的预后标志。针对这一通路,还发现了可能扩大到其他几种症状的途径,如葡萄膜炎、视神经脊髓炎和最近的COVID-19肺炎。
然而与IL-6生物学相关的问题仍未得到解答。例如,为什么会出现IL-6水平升高,为什么IL-6信号抑制会对一些与IL-6水平过高相关的疾病(如RA)患者产生有临床意义的好处,但不是所有的疾病(比如AS)都有积极作用? 回答这些问题将有助于我们进一步了解IL-6信号通路如何调节各种自身免疫疾病,并将有助于为个别患者或患者亚组开发更多的、个性化的治疗方案。如此看来,基于IL-6通路实现治疗潜力的历程还远未结束。
ACROBiosystems开发了一系列高品质的IL-6及IL-6受体蛋白,助力IL-6相关药物研发。
IL-6及IL-6受体蛋白:产品优势
多标签:Tag Free,His Tag,Avi & His Tag,Fc Tag
高生物活性经ELISA、BLI、细胞水平实验验证,免费提供Protocol


经还原条件下SDS-PAGE验证,生物素化Human IL-6 R alpha, Avitag,His Tag (Cat. No. CD6-H82E8) 纯度高于 95%。分子量计算为41.7 kDa,由于糖基化影响,经还原条件下SDS-PAGE验证分子量迁移为55-70 kDa。
验证数据:高生物活性经ELISA验证
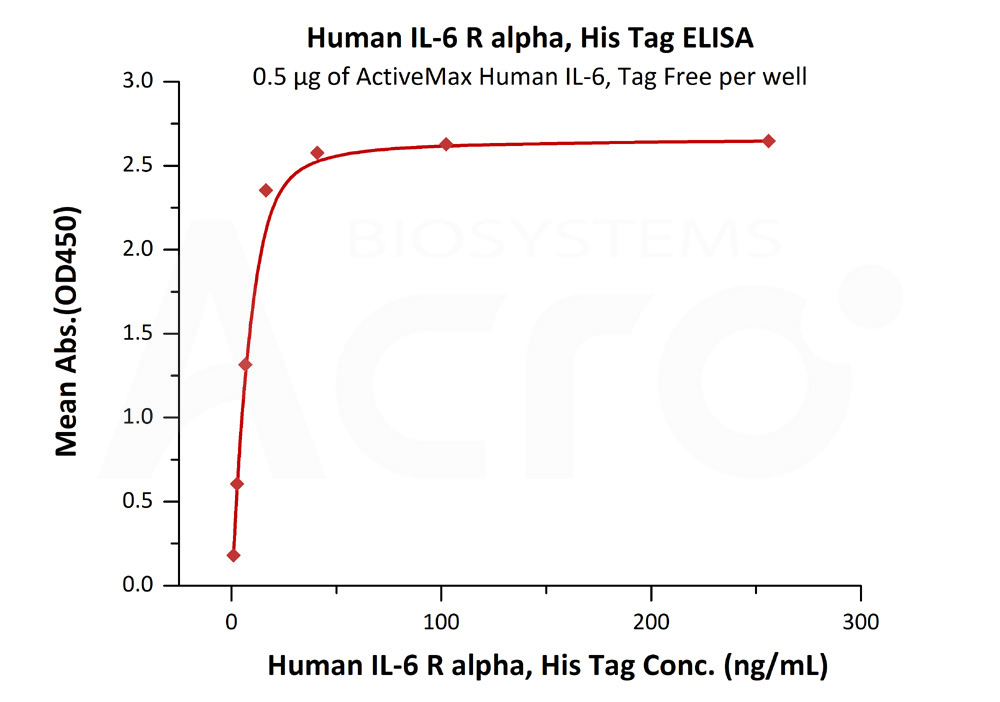
经ELISA验证,ActiveMax® Human IL-6, Tag Free (Cat. No. IL6-H4218)可特异性结合Human IL-6 R alpha, His Tag (Cat. No. ILR-H4223),线性区间为1-16 ng/mL。
验证数据:高生物活性经BLI(ForteBio Octet Red96e)验证
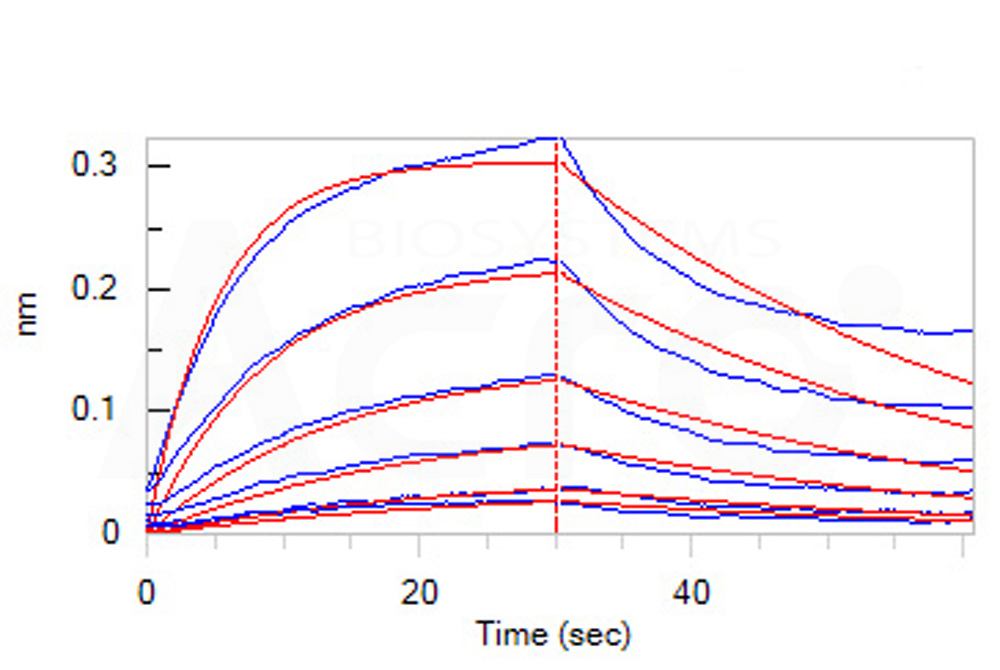
经BLI验证,装载Protein A生物传感器上的Human IL-6 R alpha, Fc Tag (Cat. No. ILR-H5259) 可以特异性结合ActiveMax® Human IL-6, Tag Free(Cat. No. IL6-H4218),亲和力常数为35.9 nM。

经细胞水平实验验证,ActiveMax® Human IL-6, Tag Free (Cat. No. IL6-H4218)可刺激TF-1 Human红白血病细胞系的增殖,EC50 为0.2856-0.3636 ng/mL。
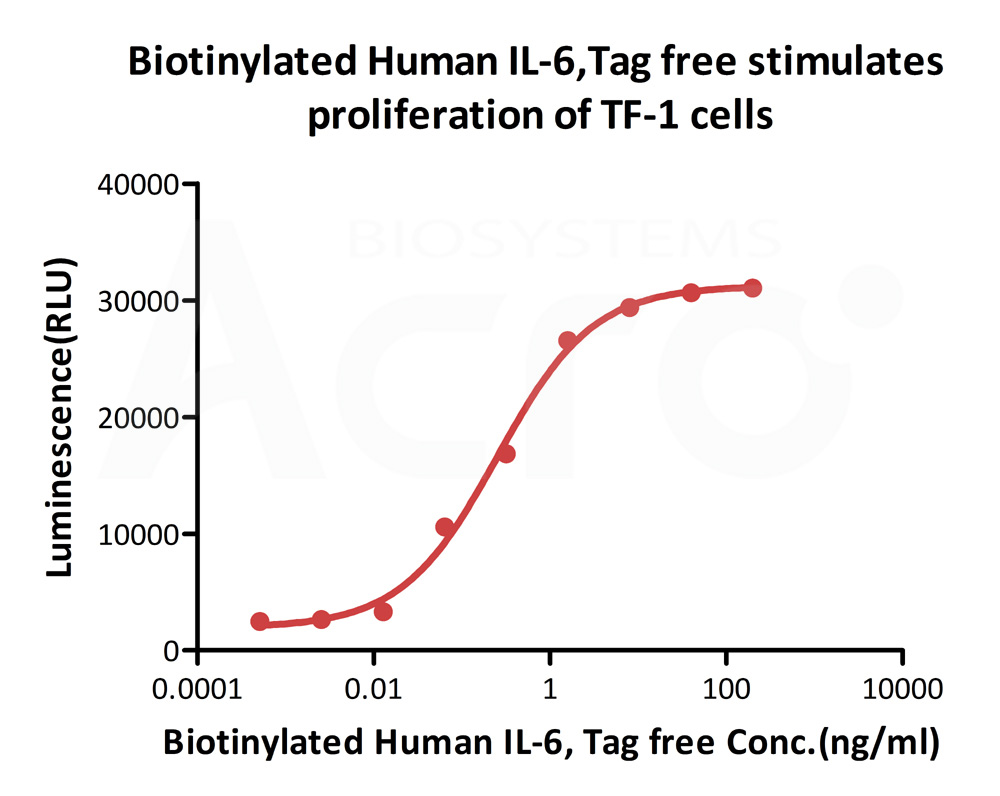
经细胞水平实验验证,生物素化Human IL-6, epitope tag free, primary amine labeling (Cat. No.IL6-H8218)可刺激TF-1 Human红白血病细胞系的增殖,EC50 为0.2532-0.4489 ng/mL。
参考文献
1. Choy, E.H., De Benedetti, F., Takeuchi, T. et al. Translating IL-6 biology into effective treatments. Nat Rev Rheumatol 16, 335–345 (2020). https://doi.org/10.1038/s41584-020-0419-z
2. Atal, S., Fatima, Z. IL-6 Inhibitors in the Treatment of Serious COVID-19: A Promising Therapy?. Pharm Med 34, 223–231 (2020). https://doi.org/10.1007/s40290-020-00342-z
3. Anjali Dhall et al. Computer-aided prediction and design of IL-6 inducing peptides: IL-6 plays a crucial role in COVID-19. Briefings in Bioinformatics. 2021, 22(2): 936–945. https://doi.org/10.1093/bib/bbaa259
4. The WHO Rapid Evidence Appraisal for COVID-19 Therapies (REACT) Working Group. Association Between Administration of IL-6 Antagonists and Mortality Among Patients Hospitalized for COVID-19: A Meta-analysis. JAMA. 2021,326(6):499–518. https://doi:10.1001/jama.2021.11330
5. Fu, B., Xu, X. & Wei, H. Why tocilizumab could be an effective treatment for severe COVID-19?. J Transl Med 18, 164 (2020). https://doi.org/10.1186/s12967-020-02339-3






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining





















