Q1:“假病毒”何以为“假”?
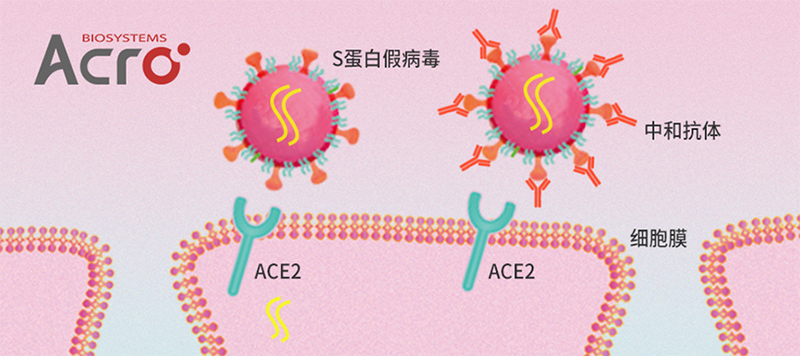
部分病毒主要由囊膜、衣壳、核酸等物质组成,其囊膜上存在的“包膜蛋白”通常与特定的细胞表面受体相互作用,促使病毒通过内吞等过程进入细胞;而病毒中的核酸包含了其遗传信息,这段核酸进入细胞后,可以指导其自身的相关蛋白合成,完成病毒的复制过程。“假病毒”的“假”主要指病毒颗粒中的核酸发生了改变,使得病毒失去复制能力,因而使得假病毒没有致病能力,较“真”病毒更加安全。一般来说,真病毒实验需要在生物安全等级3级或以上实验室开展,而假病毒实验可以在生物安全等级2级实验室中进行。对于新冠S蛋白假病毒还有第二个“假”,即病毒骨架上的包膜蛋白被替换为了新冠病毒的Spike蛋白,因而使其可以模拟新冠病毒入侵细胞的过程。
Q2:病毒骨架如何选择?
新冠S蛋白假病毒的用途是模拟新冠病毒入侵细胞,那么其性质与新冠病毒越接近,模拟程度当然就越高。如果可以的话,最理想的是使用新冠病毒作为新冠假病毒的病毒骨架。但病毒的基因组是相当复杂的,其复制组装过程也受到复杂的调控,一个可用于制备假病毒的病毒骨架的开发和技术方法的成熟化、稳定化需要一个过程。目前,HIV-1病毒骨架无疑是研究最多、成熟度最高的病毒骨架之一,例如说常用于将特定基因导入细胞基因组的“慢病毒载体”通常就是以HIV-1为骨架。当然,除了HIV-1,人们也陆续开发了多种病毒骨架,由于原始病毒本身性质不同,各个骨架的优缺点也不尽相同。在其他条件可满足的前提下,建议选择颗粒形态、大小与新冠病毒比较接近的病毒骨架制备的新冠S蛋白假病毒。当然,我们还是非常期待新冠病毒骨架的诞生。
Q3:新冠S蛋白假病毒如何包装,可以保证S蛋白的完整么?
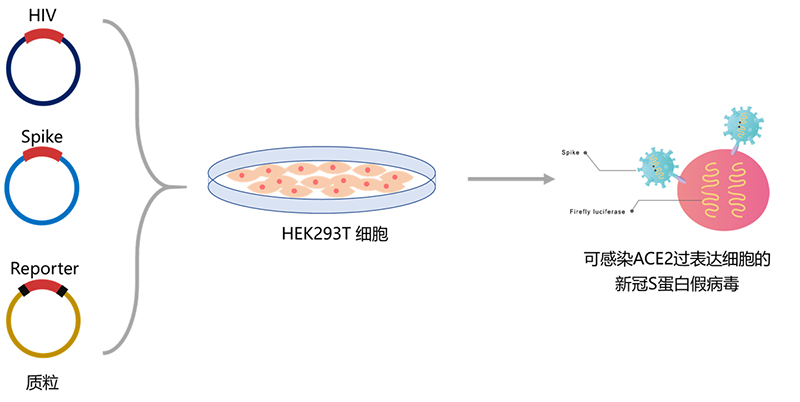
假病毒的包装即是将2、3、4甚至更多个质粒共转入HEK293T细胞中,这些质粒中含有指导病毒合成的全部基因,一段时间后,假病毒即产生。HIV-1骨架的新冠假病毒将存在于细胞培养液中,收集上清液,经过纯化即可获得新冠S蛋白假病毒悬液。
为了尽可能还原病毒入侵过程,假病毒包装过程中使用的包膜蛋白为近乎全长的新冠S蛋白基因序列,并使用人源细胞包装病毒,理论上S蛋白将在病毒包膜上呈现真实情况下的“三聚体”形式,并被糖基化,且具有构象变化的能力。考虑到新冠病毒和HIV-1病毒组装过程的差异,仅于S蛋白胞内段的片段(内质网定位信号)进行了截短以增加病毒包装效率;由于该截短与S蛋白胞外段跨膜区无关,对病毒入侵的影响较小。
Q4:新冠S蛋白假病毒安全么?
假病毒由于不能复制或感染机体更多细胞,失去了致病性,具有相对的安全性。然而实验者依然应该警惕,在生物安全2级实验室的生物安全柜中谨慎操作,皮肤或粘膜不应触碰假病毒,加样、吹吸等操作时尽量轻柔并及时关盖,以减少气溶胶的产生。实验结束后所有沾染垃圾应妥善处理。
Q5:如何比较“真”病毒实验、假病毒实验、ELISA实验?
目前真/假病毒实验、ELISA三种方法常被用于评价疫苗及抗体药物等的中和能力。
毫无疑问,真病毒实验最高程度地还原了病毒的侵染过程,但由于其较高的高危险性,需要具备生物安全等级3级或以上实验室及其他必要的资质和技术才可以开展。此外,真病毒感染细胞后,一般需要通过观察细胞病变判断感染情况,观测过程相对繁琐。
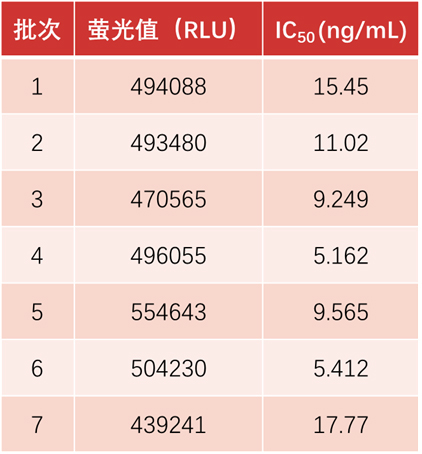
假病毒实验仅需要生物安全等级2级实验室即可开展,且假病毒在高度模拟病毒的入侵过程的同时通常都插入了一段报告基因,如萤火虫萤光素酶,这使得实验者可以很容易对病毒入侵强度进行定量。但目前的新冠S蛋白假病毒都是以其他病毒为骨架,相对于新冠真病毒会有一定的差异。
ELISA是一个基于蛋白的高度抽象化的模型,它主要模拟了病毒入侵过程中病毒包膜蛋白和受体结合的过程,相对病毒来说更为简单,所以实验的稳定性、原材料的批间差可控性均较高。但ELISA实验由于抽象程度高,离开了病毒载体等因素后一定程度引入了假阴性和假阳性。
综上,在有条件的情况下,真病毒实验是理想的选择;对于病毒入侵机制十分清楚,需要实验稳定性高的实验,ELISA可以选择;对于如新冠病毒危险性较高,或入侵机制还不十分明确的病毒,或者尽可能减少假阴性和假阳性的出现,假病毒实验是不错的选择。






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining