大多数已批准的抗体药物是IgG型免疫球蛋白,尤其IgG1居多。基于IgG1结构的药物要么是全长的IgG1抗体,要么是IgG1 Fc作为融合伴侣以延长治疗性融合蛋白的循环半衰期。这两种IgG1结构药物都可以结合和中和相同的可溶性靶标达到治疗效果,比如,可以与TNF-α结合的Etanercept/依那西普、Infliximab/英夫利昔单抗和Adalimumab/阿达木单抗,与VEGF结合的Aflibercept/阿伐西普和Bevacizumab/贝伐珠单抗,已成功用于治疗眼疾、血友病、2型糖尿病、自身免疫和癌症等一系列疾病。
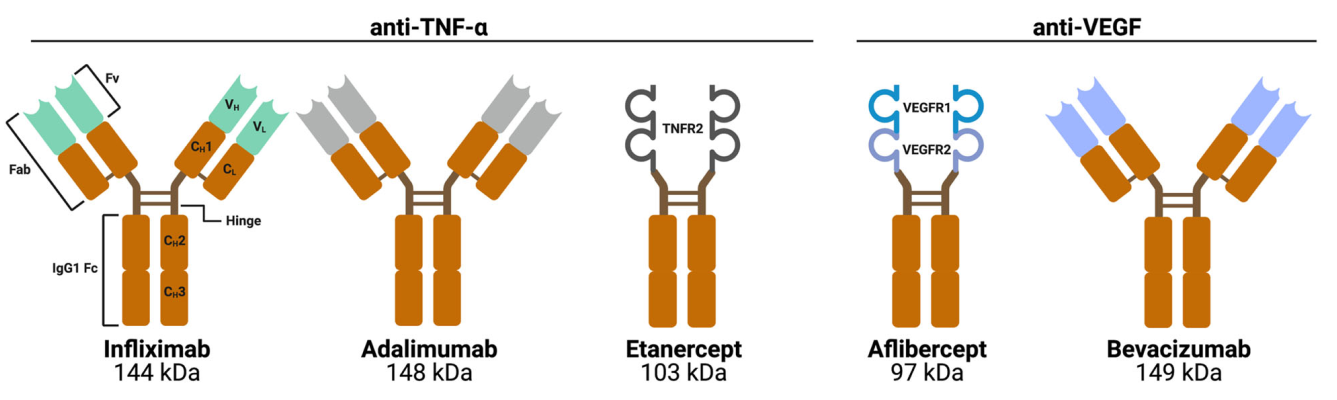
已被批准的IgG1结构药物:全长IgG1、IgG1 Fc融合蛋白
FcRn主要驻留在酸化的核内体中,在pH 5.0-6.5与IgG结合,触发复合物到细胞表面的循环,当暴露在细胞外环境的中性pH下导致配体释放,FcRn这种能够以pH依赖的方式与Fc结合,是全长IgG1抗体和IgG1 Fc融合蛋白药物循环半衰期的关键调节因子。
更长的血浆半衰期能够延长给药间隔,增加治疗依从性。一般来说,IgG1抗体半衰期从6天到32天不等,平均半衰期为3周;而大多数IgG1 Fc融合药物的半衰期比全长IgG1短得多,如etanercept、eftrenonacog alfa和romiplostim的平均半衰期低于5天。
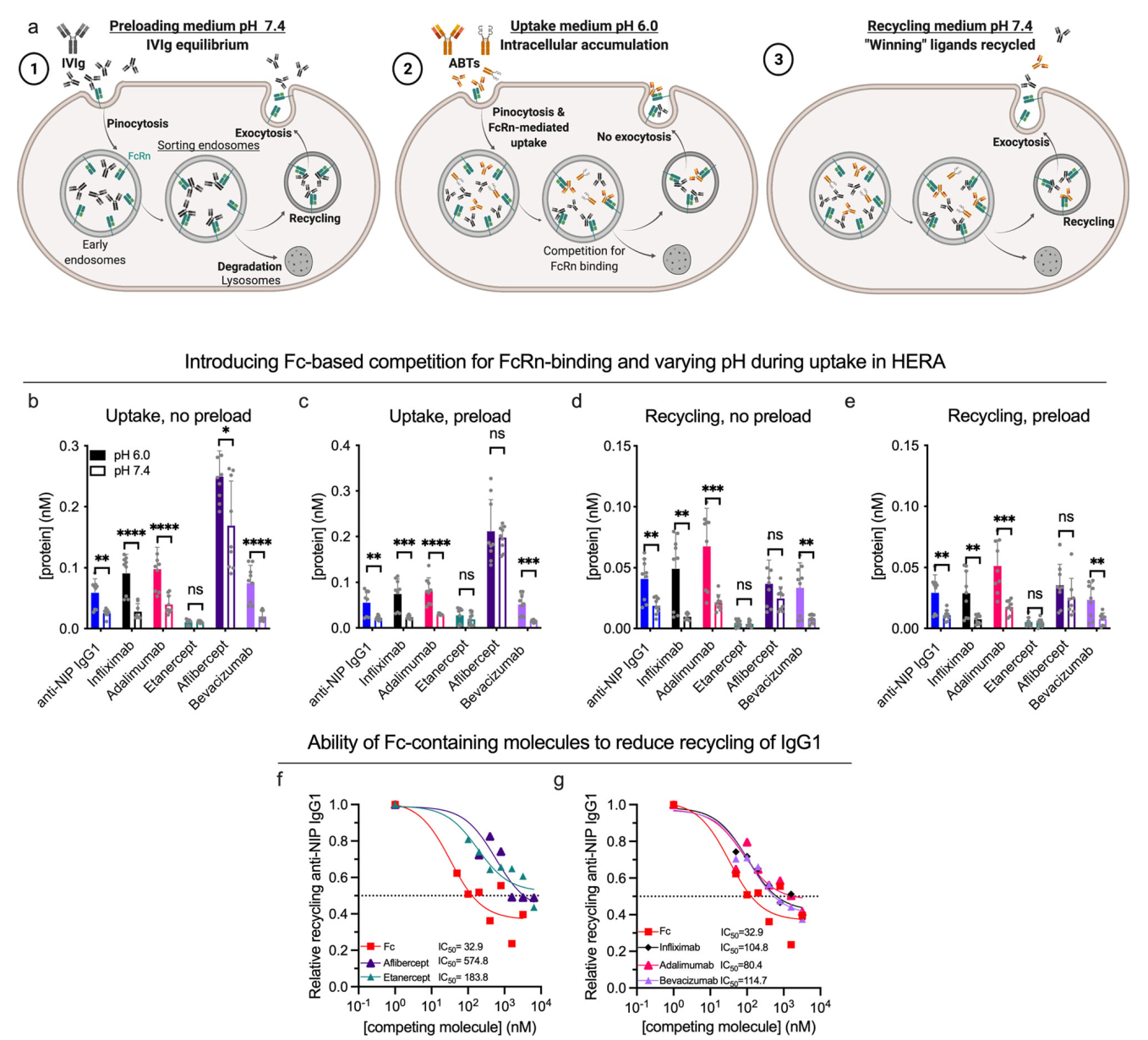
鉴于IgG1和Fc融合蛋白与FcRn结合的能力及其细胞运输特性尚不清楚,Oslo大学和Roche团队日前发表了《Biophysical differences in IgG1 Fc-based therapeutics relate to their cellular handling, interaction with FcRn and plasma half-life》一文,对全长IgG1抗体和IgG1 Fc融合蛋白的FcRn衔接和细胞运输进行了全面研究和报道。
他们发现,即使是具有相同Fc序列及FcRn主要结合位点的IgG1结构药物,仍具有明显的生物物理差异,表现出不同的半衰期,这并不是源于与受体体外结合动力学的差异(因为它们在SPR中结合是相当的),而是FcRn依赖性和非依赖性因素共同作用的结果。尽管FcRn的主要结合位点位于Fc区域,但Fab臂仍可参与调节,并可能直接与受体相互作用; 此外,IgG结构药物的生物物理特性,如等电点(PI)和表面电荷分布,可以调节靶结合和血浆半衰期,净正电荷可能导致与带负电荷的细胞膜的非特异性相互作用和脱靶结合,而抗原相互作用残基中的表面正电荷可能延迟FcRn的释放。为了在细胞环境中比较,研究团队采用人类内皮细胞的循环试验(HERA,human endothelial cell-based recycling assay)发现:IgG1 Fc片段可通过依赖于FcRn的机制被有效地内化、回收和跨细胞,相比之下,这些机制对IgG1的作用效率较低,尽管IgG1 Fc片段被大量吸收和循环利用,但由于摄取的增加大于回收,IgG1 Fc片段在细胞内积累而被降解,可以部分解释为何IgG1 Fc融合蛋白血清半衰期更短。另外IgG1结构药物会与内源性IgG竞争与FcRn的结合,而IgG1 Fc融合蛋白在细胞回收方面的竞争力不如IgG1。
pH值和细胞回收竞争对抗体结构药物有不同的影响
从方法学的角度来看,该研究团队总结揭示了研究FcRn介导过程必须仔细考虑两大因素——(1)受体嵌入细胞膜,结合动力学与细胞运输之间缺乏相关性;(2)FcRn上IgG1结合位点的竞争压力,IgG1 Fc融合蛋白的回收效率受损,在FcRn作用中产生较差的竞争能力——进而预测IgG1 Fc结构药物与FcRn相互作用的性质和结果。
为助力IgG结构药物开发,ACROBiosystems百普赛斯可为您提供ComboXTM通用型研发工具:同型对照系列产品IgG Fc。我们的IgG Fc重组蛋白仅包含了铰链区、CH2、CH3序列,而不包含Fab序列,可以作为单抗、IgG样双抗、ADC药物及融合IgG Fc药物的同型对照,应用于药物筛选、功能验证、生物学活性检测、有效性及安全性评估等药物开发场景。(此外,IgG Fc蛋白可以作为内源性IgG,与靶向FcRn药物进行结合FcRn的竞争性实验验证。)
IgG Fc产品覆盖不同标签的Human IgG1 Fc(包含突变及非突变设计)、IgG2 Fc、IgG3 Fc、IgG4 Fc,Mouse IgG1 Fc、IgG2a Fc、IgG2b Fc,Llama IgG2b Fc,Rabbit IgG Fc。
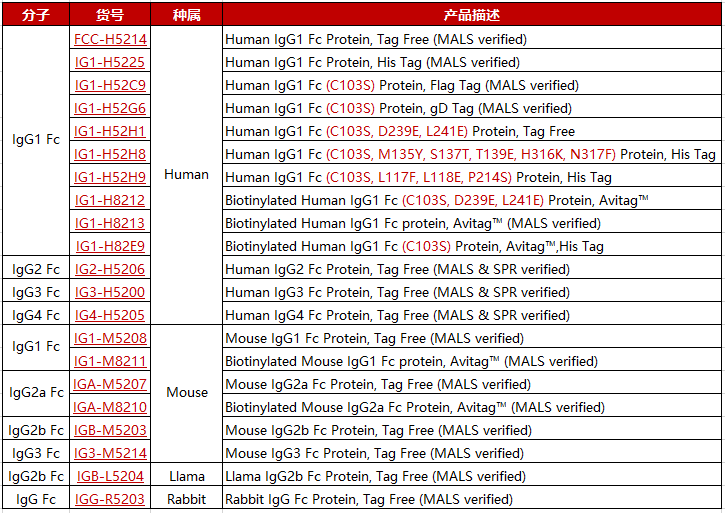
点击图片查看更多产品详情
✍ 高纯度及结构均一度经SDS-PAGE&SEC-MALS验证
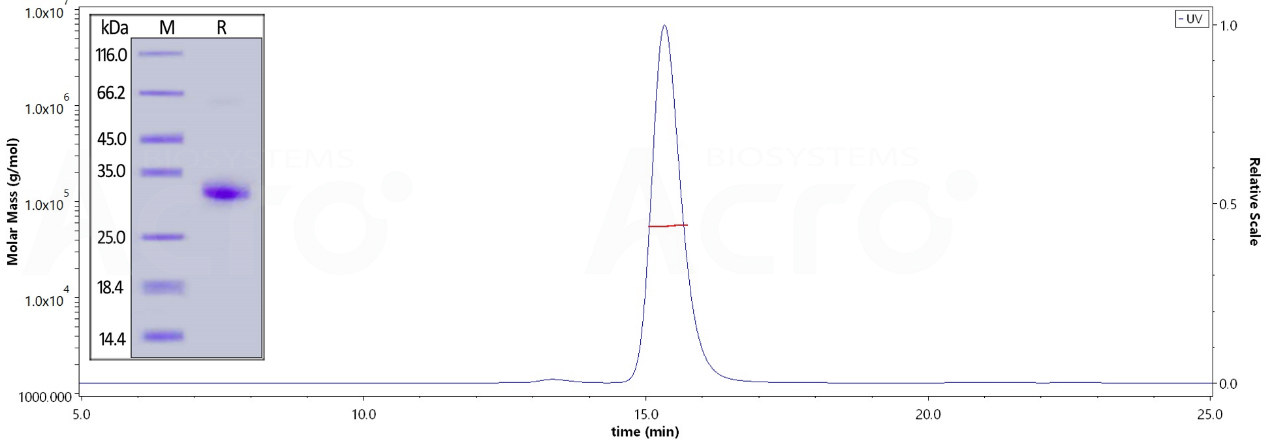
经还原条件下SDS-PAGE验证,人源IgG1 Fc, Tag Free(Cat. No. FCC-H5214) 纯度高于95%;经SEC-MALS验证,其纯度高于90%,分子量为50-65kDa(二聚体)。
✍ 高生物活性经ELISA&SPR验证
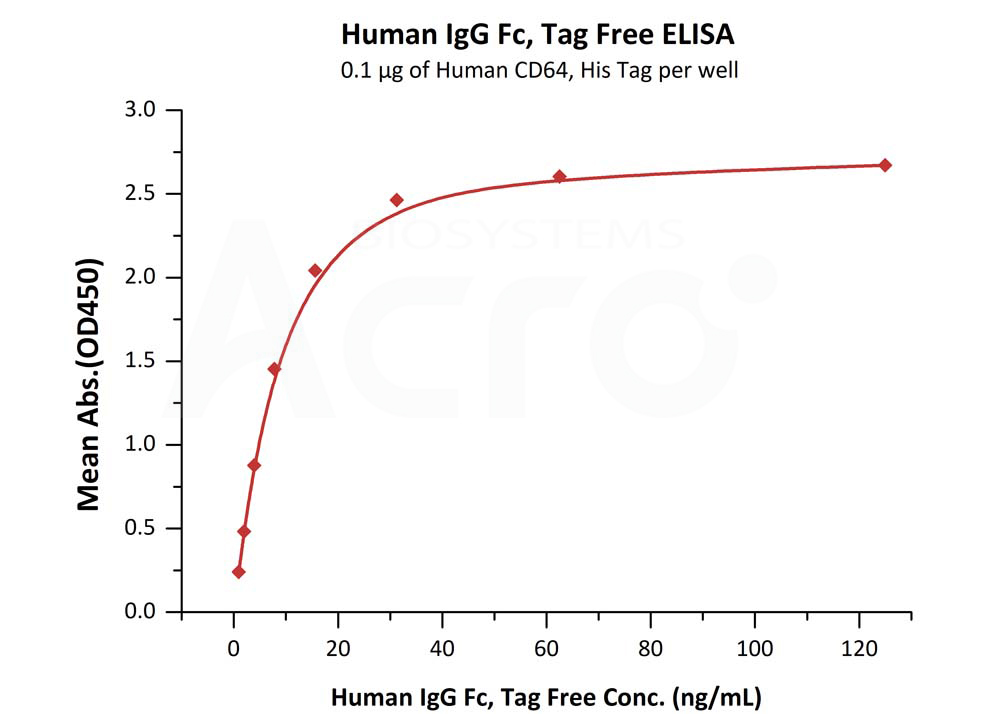
经ELISA验证,人源CD64, His Tag (Cat. No. FCA-H52H1) 可与人源IgG1 Fc, Tag Free (Cat. No. FCC-H5214) 特异性结合,线性区间为1-16 ng/mL。
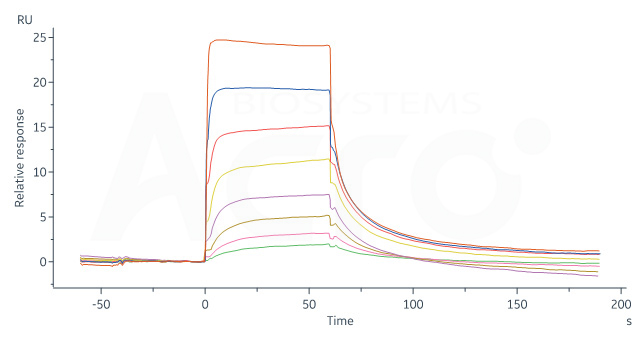
经SPR验证,人源FCGRT&B2M异源二聚体蛋白, His Tag (Cat. No. FCN-H52W7) 可以通过捕获在CM5芯片上的抗anti-His 抗体与人源IgG1 Fc, Tag Free (Cat. No. FCC-H5214) 特异性结合,亲和力常数为0.957 μM (Biacore 8K)。
✍ IgG Fc作为同型对照,验证同亚型的单克隆抗体与靶点抗原结合的特异性
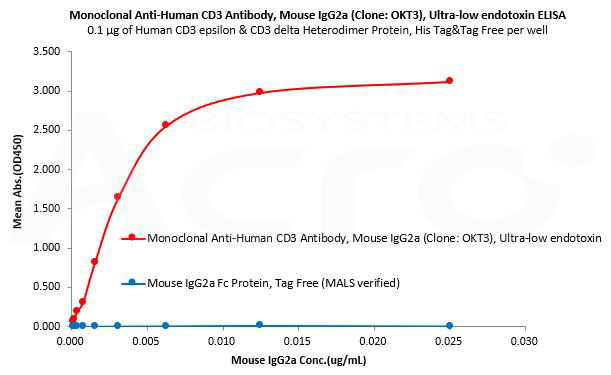
经ELISA验证,Human CD3 epsilon & CD3 delta Heterodimer Protein, His Tag&Tag Free (MALS verified) (Cat. No. CDD-H52W1) 可与Monoclonal Anti-Human CD3 Antibody, Mouse IgG2a (Clone: OKT3), Ultra-low endotoxin (Cat. No. CDE-M120a) 特异性结合,线性区间为0.2-3 ng/mL, 与Mouse IgG2a Fc Protein, Tag Free (MALS verified)(Cat. No. IGA-M5207) 不结合。
1. Gjølberg, T.T., Frick, R., Mester, S. et al. Biophysical differences in IgG1 Fc-based therapeutics relate to their cellular handling, interaction with FcRn and plasma half-life. Commun Biol 5, 832 (2022). https://doi.org/10.1038/s42003-022-03787-x






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining