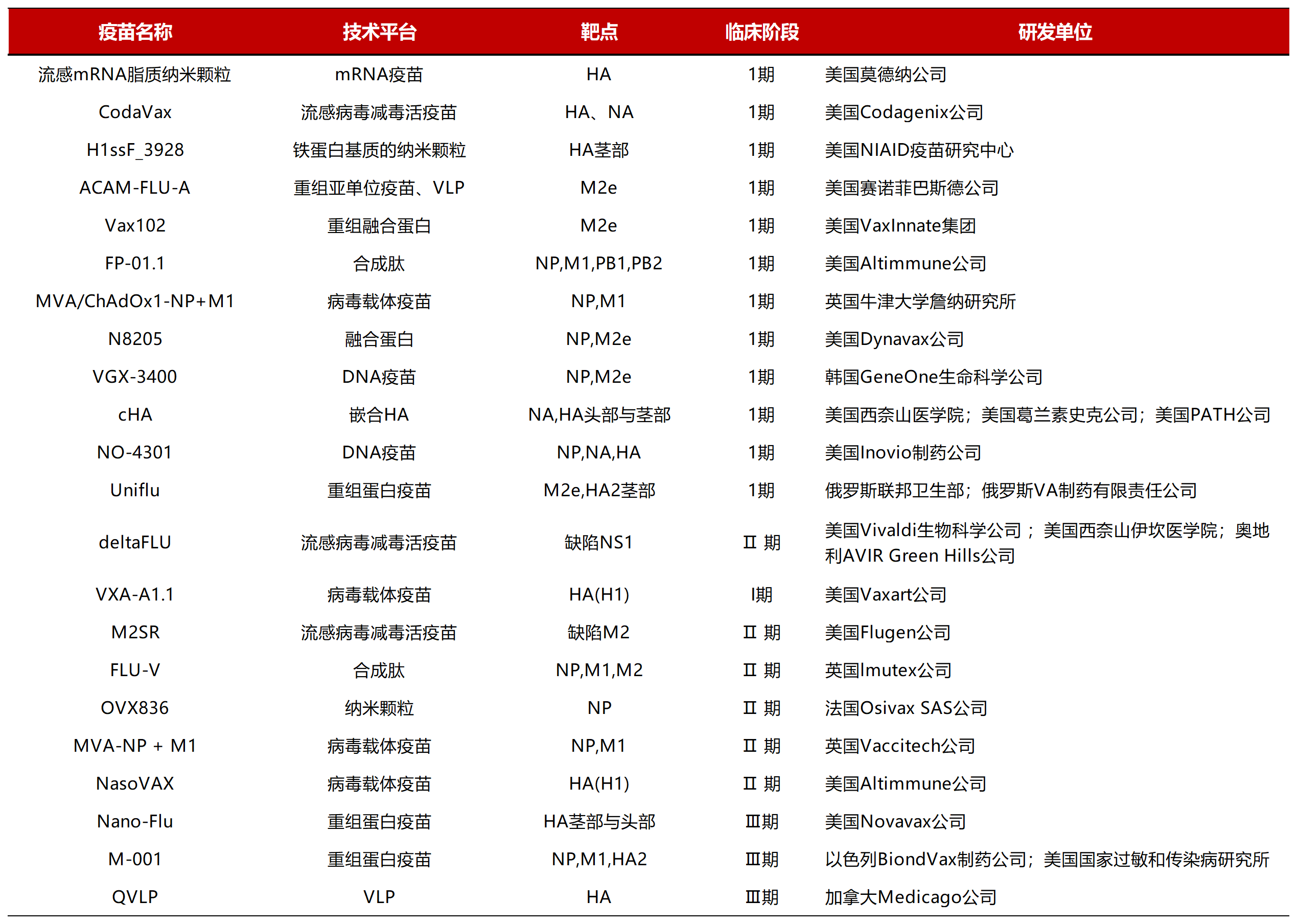
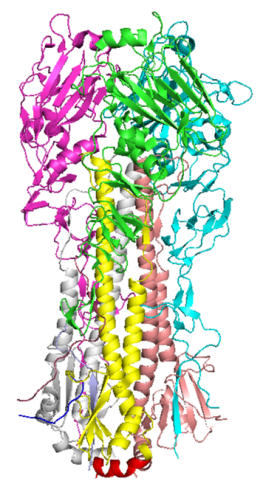
血凝素(Hemagglutinin,HA)是流感病毒包膜表面含量最多的糖蛋白,在病毒侵袭和感染过程中起关键作用,天然以三聚体(Trimer)的形式存在于双层类脂膜上,每个HA单体又由球状头部和杆状茎部两部分组成:球状头部由HA1组成,负责病毒与宿主细胞表面唾液酸受体的结合,将病毒吸附到宿主细胞表面;杆状茎部由HA2和部分HA1组成,并锚定在病毒衣壳的脂质双层中,HA2主要介导病毒包膜与宿主细胞膜的融合。病毒通过内吞作用进入宿主细胞后,在低pH诱导下,实现由膜融合前状态(pre-fusion)到膜融合后状态(post-fusion)的转变,从而完成病毒与宿主细胞膜的融合。
HA头部含有抗原决定簇和受体结合位点,是疫苗开发的重要靶抗原,目前的季节性疫苗也主要触发针对HA头部结构域的抗体;然而,该位点容易发生抗原漂移和转化,导致疫苗保护有限。高度保守的HA茎产生保护性抗体,在不抑制血凝作用的情况下中和病毒感染性,是开发通用流感疫苗更具吸引力的目标。许多研究表明,该位点含有许多结合广谱中和抗体(bnAbs)的抗原表位,并且在抑制病毒进入细胞中具有重要作用。
HA2区是通用流感疫苗的潜在研究靶点,但由于HA茎的抗原表位经常被其头部阻断,疫苗设计需要增加HA茎对宿主免疫系统的暴露,例如通过使用茎结构域中的某些短肽表位与载体蛋白结合以增加HA茎的免疫暴露和帮助抗原呈递到茎的结构域,从而增强免疫作用。
通用流感疫苗研发中极具潜力的靶标:神经氨酸酶(NA)

神经氨酸酶(Neuraminidase,NA)是流感病毒包膜表面含量仅次于HA的糖蛋白,主要通过切割宿主细胞膜上的病毒唾液酸受体来促进病毒颗粒的释放并防止后代病毒在细胞表面的积累,从而在病毒传播中起重要作用。NA从N端到C端可分为四个主要区域:细胞质区、跨膜区、茎区和头部区。
目前季节性流感疫苗主要靶向HA,然而,美国疾控中心数据显示,最近10年流感疫苗在北美的平均保护率只有40%,研究表明[2],流感疫苗由于缺少NA的有效表位,所以疫苗接种人群中很难诱导出有效的NA特异性的体液免疫应答,相反,流感病毒自然感染患者却能诱导高比例的NA的抗体应答。这些抗体在体外实验中不仅显示出广谱与高效的抗病毒活性,还具有抑制“达菲”耐药流感病毒株感染复制的能力。进一步研究证实,NA抗体不止能分别保护小鼠免受10倍致死剂量的季节性流感毒株H1N1与H3N2的感染,还能抵制禽流感H5N1的致命感染。可见,NA是未来的新型通用型流感疫苗研究极具潜力的重要靶点。
除HA和NA外,流感病毒基质蛋白2的细胞膜外区(M2e)和核蛋白(NP)因其在任何亚型的人类流行性病毒株中均高度保守,被提出可作为通用疫苗设计的候选免疫原。
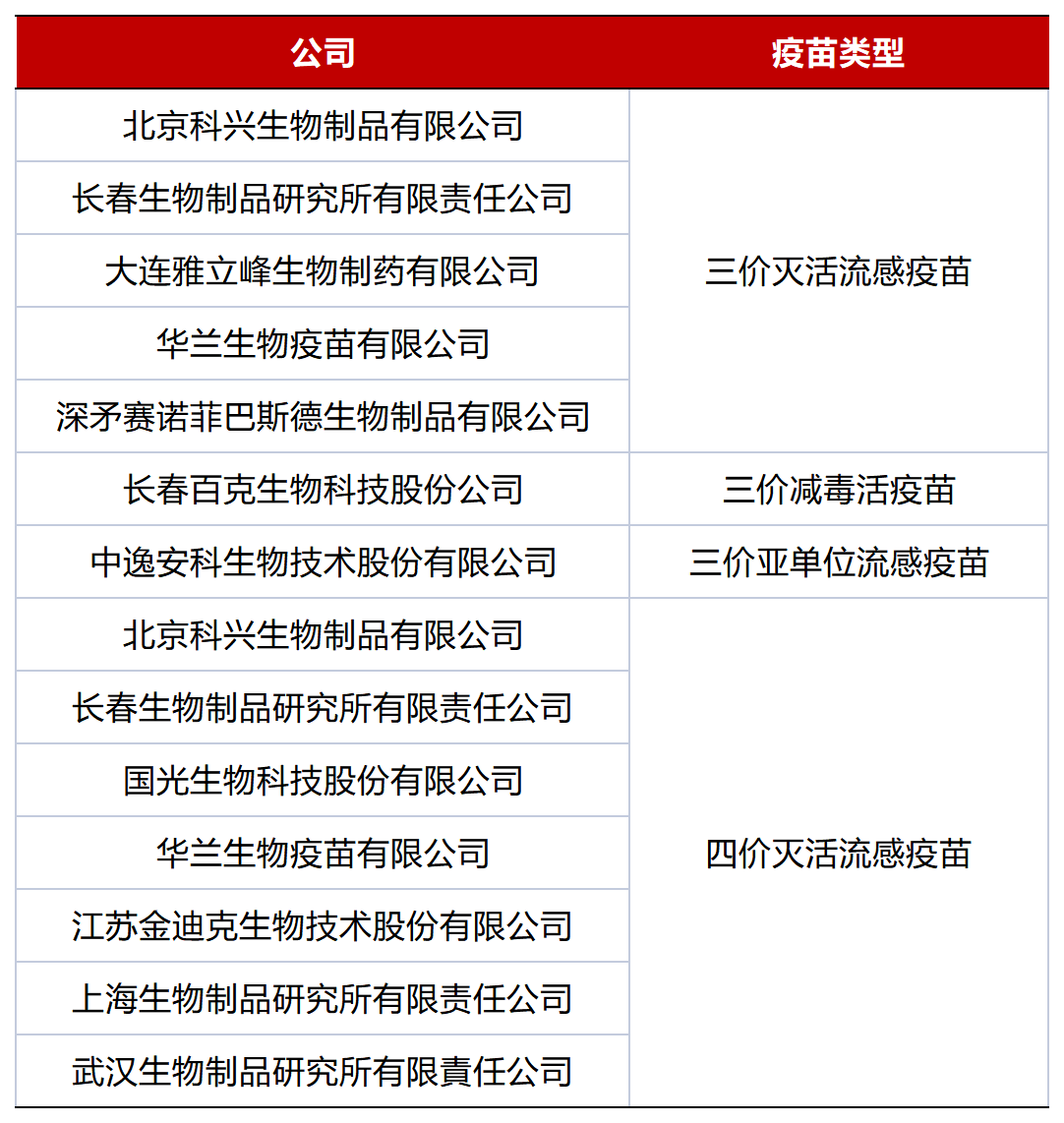
为支持流感疫苗的研究开发,ACROBiosystems特开发了流感病毒不同亚型的HA及NA靶点蛋白,可用于各种类型流感疫苗的开发与质量控制阶段,力求加快其研究进程。
● 覆盖2022-2024年流行毒株及H5Nx多亚型;
● 提供HA天然三聚体构象蛋白、NA四聚体构象蛋白等不同疫苗研发所需抗原;
● His、His & Avi等不同标签可供选择,满足不同实验设计需求;
● HA纯度经SDS-PAGE及MALS验证,大于90%;生物活性经抗体结合实验验证。
验证数据:
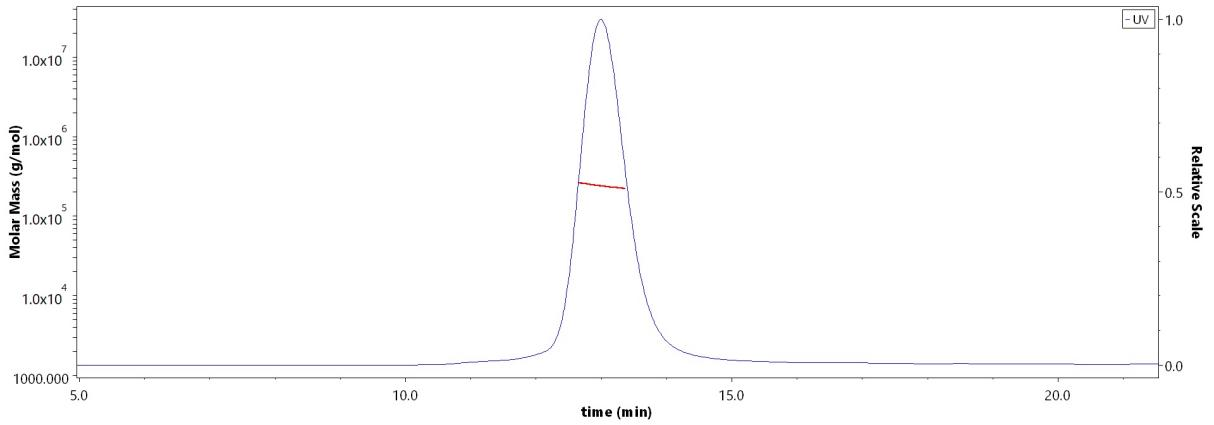
The purity of Influenza A [A/Darwin/6/2021 (H3N2)] HA Protein, His Tag (Cat. No.HA2-V52H5) is more than 90% and the molecular weight of this protein is around 225-255 kDa verified by SEC-MALS.

Immobilized Influenza A [A/Darwin/6/2021 (H3N2)] Hemagglutinin (HA) Protein, His Tag (Cat. No.HA2-V52H5) at 1 μg/mL (100 μL/well) can bind Human Anti-HA (H3N2) antibody CR8020 Human IgG1 with a linear range of 0.4-25 ng/mL (QC tested).
>> 为了更好的支持广大流感疫苗研发需求,ACROBiosystems还可以提供流感假病毒产品及检测服务,全面助力传染病相关研究与疫苗及药物研发,欢迎点击咨询。

ACROBiosystems密切关注着多种病毒、传染性疾病的发展态势,陆续研发了多种包膜病毒和非包膜病毒的报告基因假病毒,并基于报告基因假病毒产品,推出假病毒研究相关技术服务,为传染病药物研发领域客户提供抗体及其他抗病毒药物的筛选和评价、中和抗体检测以及疫苗效价评估,助力疫苗、诊断及治疗性药物的开发。
参考文献
[1] Li J, Zhang Y, Zhang X, Liu L. Influenza and Universal Vaccine Research in China. Viruses. 2022 Dec 30;15(1):116. doi: 10.3390/v15010116. PMID: 36680158; PMCID: PMC9861666.
[2] Piepenbrink M S , Nogales A , Basu M ,et al.Broad and Protective Influenza B Virus Neuraminidase Antibodies in Humans after Vaccination and their Clonal Persistence as Plasma Cells[J].Mbio, 2019, 10(2).DOI:10.1128/mBio.00066-19.






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining