ADAM(A
Disintegrin and
Metalloproteinase,ADAMs)家族是一类多功能的锌依赖性金属蛋白酶,它们通过剪切细胞表面的膜结合分子来调节信号传导,并参与蛋白水解、细胞粘连和细胞融合等过程。组织修复、免疫反应、生殖和神经系统发育中,ADAM家族扮演着关键角色。人类基因组中已鉴定出超过20种ADAM家族成员,其中13种具有蛋白水解活性。这些成员在不同组织和细胞类型中表达,并且与多种生理和病理过程相关,包括与疾病相关的异常表达。
ADAM家族蛋白的激活通常涉及前肽域的移除,这一过程对于大多数ADAM成员至关重要。然而,某些成员如ADAM-12可以在不移除前肽的情况下保持活性,这表明ADAM家族中存在功能上的多样性。在体内,ADAM成员的分布和功能各异,一些与生殖过程相关,如ADAM-1、2、3,而另一些如ADAM-8、9、10、15和17则在心血管发育中发挥作用,并可能与心血管疾病的发生有关。
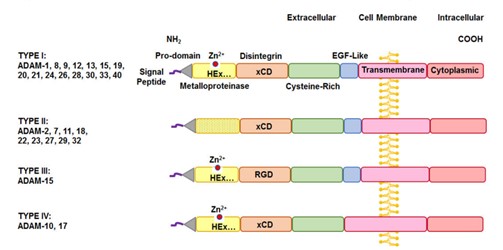
ADAM 家族不同类型之间的序列差异
最新研究表明,ADAM家族成员的活性和表达模式在不同疾病中可能有所不同,这为开发新的治疗策略提供了潜在的靶点。
ADAM-8在多种病理状态中发挥作用,如类风湿性关节炎、哮喘和炎症。它还参与调包括排卵、破骨细胞分化和中性粒细胞活动等生理过程。在人类细胞中,ADAM-8通常储存在颗粒中,刺激后可移动到细胞表面。ADAM-8也参与细胞粘附和迁移过程。
为了探究ADAM-8的功能,研究人员开发了一种缺乏活性的ADAM-8突变小鼠模型,结果表明这种突变可以抑制自身免疫性关节炎的发展。尽管ADAM-8缺失的小鼠(ADAM-8−/−)能够正常发育成长并且没有明显的疾病表型,但ADAM-8似乎在心脏炎症中发挥作用,因为在心肌梗死后的边缘区域,ADAM-8的水平会上升,这与炎症细胞的浸润相关。
ADAM9是一种1型ADAM蛋白,在肿瘤的发生和发展中扮演重要角色。它在多种癌症中过度表达,如肺癌、前列腺癌和乳腺癌,并且其高表达水平与患者的不良预后有关。ADAM9通过增强肿瘤的侵袭性和迁移能力,促进了疾病的进展。特别是在肺癌中,高水平的ADAM9表达与更高的脑转移风险和较短的总生存期相关联。除了在肿瘤学中的作用外,ADAM9还参与了HB-EGF的脱落,并可能通过减少APP加工来对抗阿尔茨海默病的发展。
在治疗性药物开发方面,ADAM9已成为一个有吸引力的治疗靶点。IMGC936曾是最早进入临床试验的抗ADAM9抗体药物偶联物(ADC),但由于未能达到预期的安全性和有效性标准,导致开发合作终止。MacroGenics公司正在开发另一种名为MGC028的ADAM9
ADC药物,该药物使用了来自Synaffix公司的可裂解linker技术,旨在提高药物的稳定性。MGC028的有效载荷是拓扑异构酶I抑制剂SYNtecan
E,药物抗体比(DAR)约为4。在2024年的AACR会议上,MacroGenics展示了MGC028的临床前数据,显示其在多个患者衍生的异种移植(PDX)肿瘤模型中具有抗癌活性。该公司计划在今年晚些时候申请开展人体试验。
另外,由ImmunoGen开发的AEX-6003也是一种针对ADAM9的ADC药物,使用了可裂解连接子SPDB和Maytansinoid DM4作为毒素部分,目前仍处于临床前阶段,详细信息尚未完全公开。
ADAM-10是参与胚胎发育、细胞外基质降解、细胞表面蛋白的胞外域脱落以及远端细胞信号调节的关键蛋白。它是Notch和Eph/ephrin信号途径的重要调节因子,通过调控Notch受体的裂解和随后的受控膜内蛋白水解(RIP),影响胞内域的核转运和基因转录。ADAM-10对Notch信号的调节在心血管系统的发育中至关重要。由于其在RIP、Notch/Delta信号传导和APP加工中的核心作用,ADAM-10敲除小鼠在早期胚胎阶段无法存活,并且表现出类似于Notch/Delta信号缺失小鼠的多系统缺陷。
ADAM-10在多种肿瘤中过表达,并通过释放生长因子、细胞因子和粘附分子等方式影响癌症进程。这些释放的蛋白质能激活其他细胞上的相应受体,触发促癌信号通路。例如,ADAM-10作为EGF和betacellulin的脱落酶,激活EGFR/HER家族受体,进而激活下游的促增殖途径。因此,在多种肿瘤类型中视ADAM-10为潜在的生物标志物。
ADAM-15通过切割E-cadherin来破坏上皮和内皮细胞间的连接,这减少了细胞间的联系和组织的稳定性。这种破坏作用促进了心血管系统中炎性细胞的迁移和浸润,增加了内皮细胞的通透性,促进了中性粒细胞的跨内皮迁移和炎症细胞的浸润。
ADAM-15还参与了心血管疾病的发展,如动脉粥样硬化、心肌炎和心肌梗死。它通过激活Src激酶和磷酸化ERK1/2来降低内皮细胞的稳定性。此外,ADAM-15与血管生成有关,能够诱VEGF及其受体VEGFR1和VEGFR2的表达,这些都是血管生成的关键因素。
在癌症转移方面,ADAM-15能够增加肿瘤细胞的迁移性和侵袭性。虽然ADAM-15基因敲除小鼠没有明显的表型,但这些小鼠的肿瘤细胞在迁移和侵袭方面的能力有所降低,表明ADAM-15在肿瘤转移过程中可能发挥作用。
总之,ADAM-15在心血管疾病和癌症转移中扮演着重要角色,是一个潜在的治疗靶点。
ADAM17是所有ADAM蛋白中研究最广泛的ADAM17,也称为TNFα转换酶或TACE,在调节细胞信号传导、参与胚胎发育、心血管疾病、肿瘤发展、炎症反应以及神经生物学等多个关键生物学及病理过程中发挥重要作用。它通过切割细胞表面的膜结合分子如TNFα和EGF家族成员来调控细胞行为,其活性的异常变化与动脉粥样硬化、心肌梗死、心脏衰竭等心血管疾病以及肿瘤生长和转移有关。因此,ADAM17不仅在疾病机制研究中占有重要地位,也是药物开发中一个具有广泛治疗潜力的靶点,针对它的抑制剂可能对治疗自身免疫疾病和癌症等疾病具有重要意义。
近日,“Signal Transduction and Targeted Therapy”(IF=40.8)上发表了一篇题为“Targeting
a disintegrin and metalloprotease (ADAM) 17-CD122 axis enhances CD8+ T
cell effector differentiation and anti-tumor immunity”的文章。这篇文章探讨了ADAM17在调控CD8+ T细胞效应分化和抗肿瘤免疫中的作用。
结果表明ADAM17通过剪切CD122分子来抑制CD8+ T细胞的免疫反应和功能,而靶向ADAM17能显著增强CD8+ T细胞的效应功能和抗肿瘤活性,抑制ADAM17可以提高CAR-T细胞在实体瘤中的疗效。这些发现为开发针对ADAM17的癌症免疫治疗策略提供了新的视角。
随着对ADAM家族成员功能和调控机制的深入了解,它们被视为治疗相关疾病的潜在靶点。研究者正在开发针对特定ADAMs的抑制剂,以期用于临床治疗。
ACROBiosystems百普赛斯根据市场需求和研究现状,推出ADAM家族蛋白产品,产品高纯度经SDS-PAGE验证,可用于抗体筛选、表征、一致性评价, 充分满足药物研发的需求,助力抗体药物临床申报。
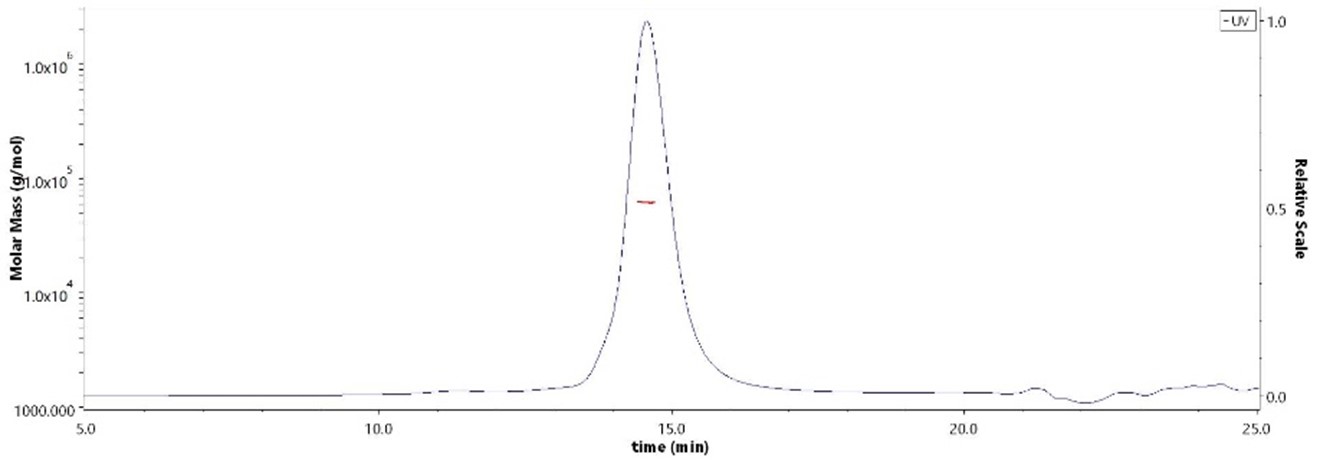
The purity of Biotinylated Human ADAM9, His,Avitag (Cat. No. AD9-H52E1) is more than 90% and the molecular weight of this protein is around 50-70 kDa verified by SEC-MALS.
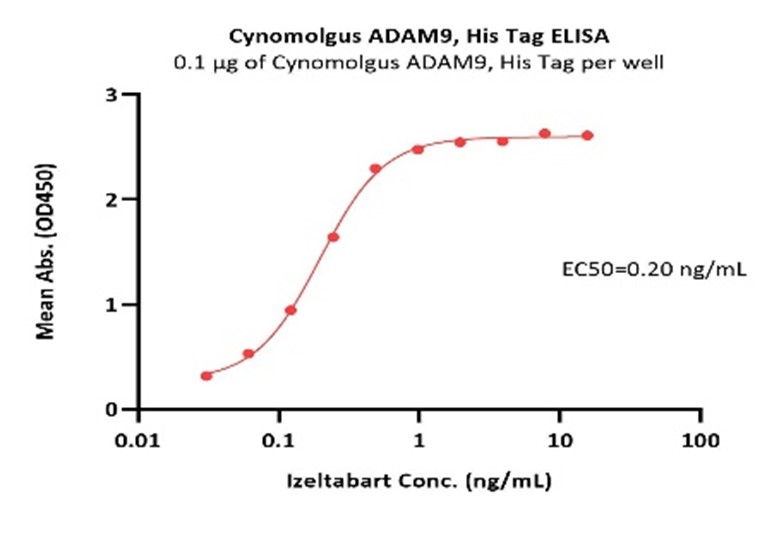
Immobilized Cynomolgus ADAM9, His Tag (Cat. No. AD9-C52H7) at 1 μg/mL (100 μL/well) can bind Izeltabart with a linear range of 0.03-1 ng/mL (QC tested).
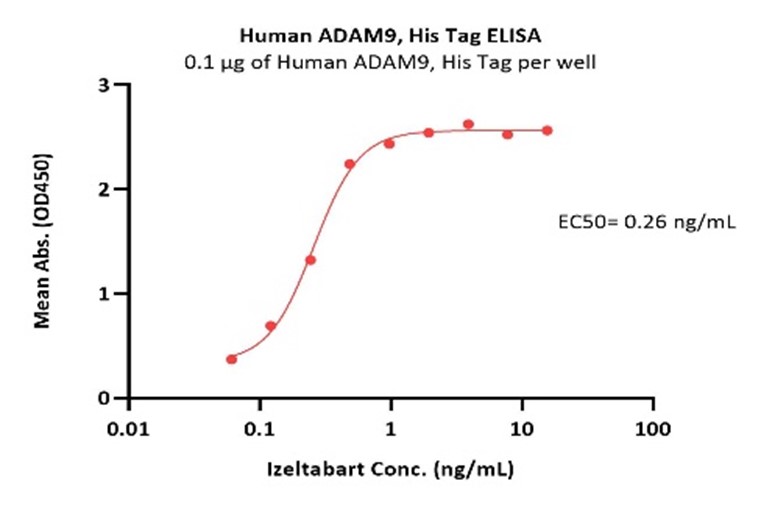
Immobilized Human ADAM9, His Tag (Cat. No. AD9-H52H7) at 1 μg/mL (100 μL/well) can bind Izeltabart with a linear range of 0.06-1 ng/mL (QC tested).






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining