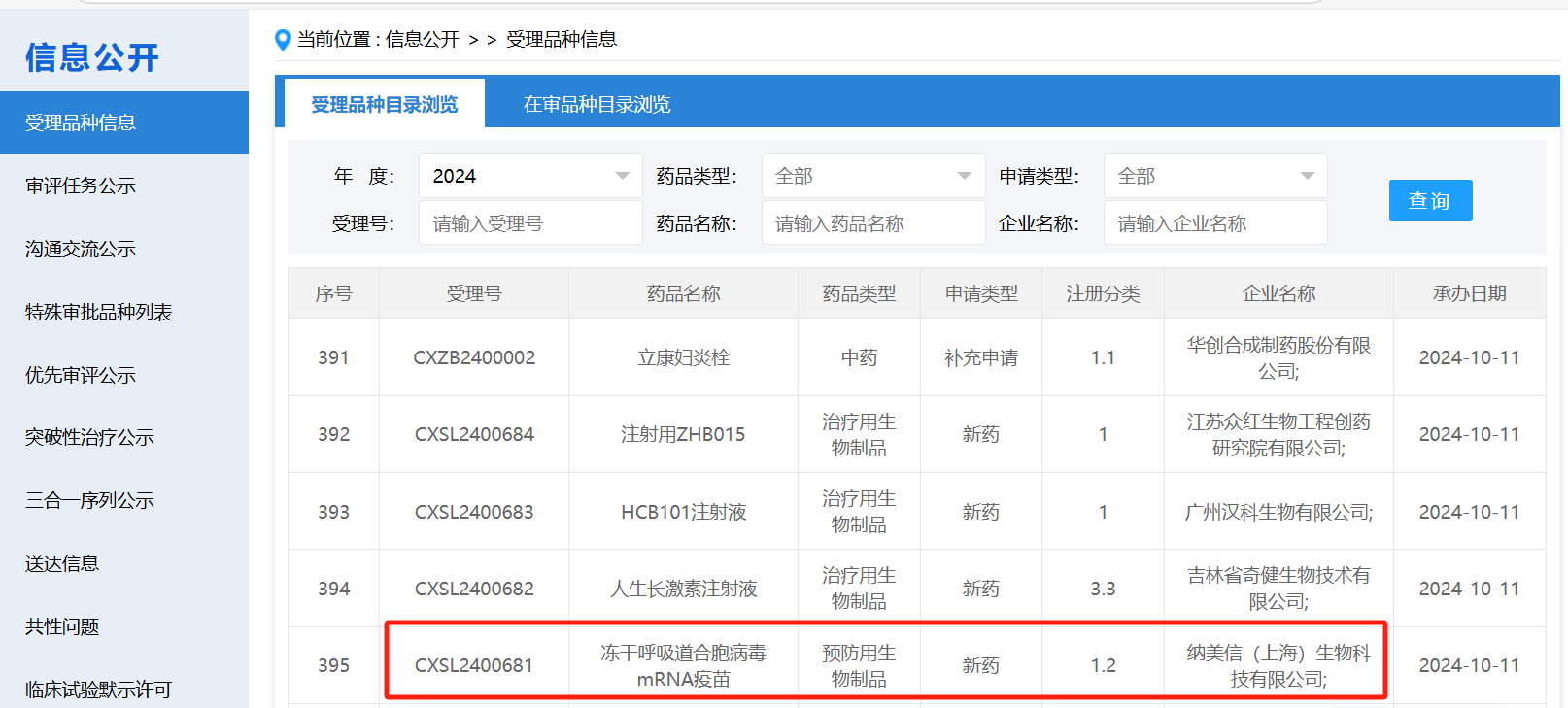
2024年10月11日,据国家药品监督管理局药品审评中心(CDE)官网公示,纳美信(上海)生物科技有限公司(“纳美信”)申报的冻干呼吸道合胞病毒mRNA疫苗NR222新药临床试验申请(受理号:CXSL2400681)获受理。纳美信专注于mRNA相关技术领域的新型疫苗/药物研发,其冻干呼吸道合胞病毒mRNA疫苗NR222是国内公开申报临床的首款冻干剂型RSV
mRNA疫苗,也是纳美信申报的首款mRNA疫苗,NR222通过增加特异性氨基酸序列等设计、优化,增强了preF抗原的免疫原性和结构稳定性。
疫苗制品在原液、半成品、成品阶段需要对病毒抗原含量进行检测,且各阶段需要符合不同的要求。《中国药典》明确规定使用ELISA法进行疫苗制品的病毒抗原检测[1]。ELISA技术还可用于疫苗制品的抗原表达率、病毒滴定、铝吸附效果测定试验及铝吸附完全性试验等类别试验中的病毒抗原含量测定。
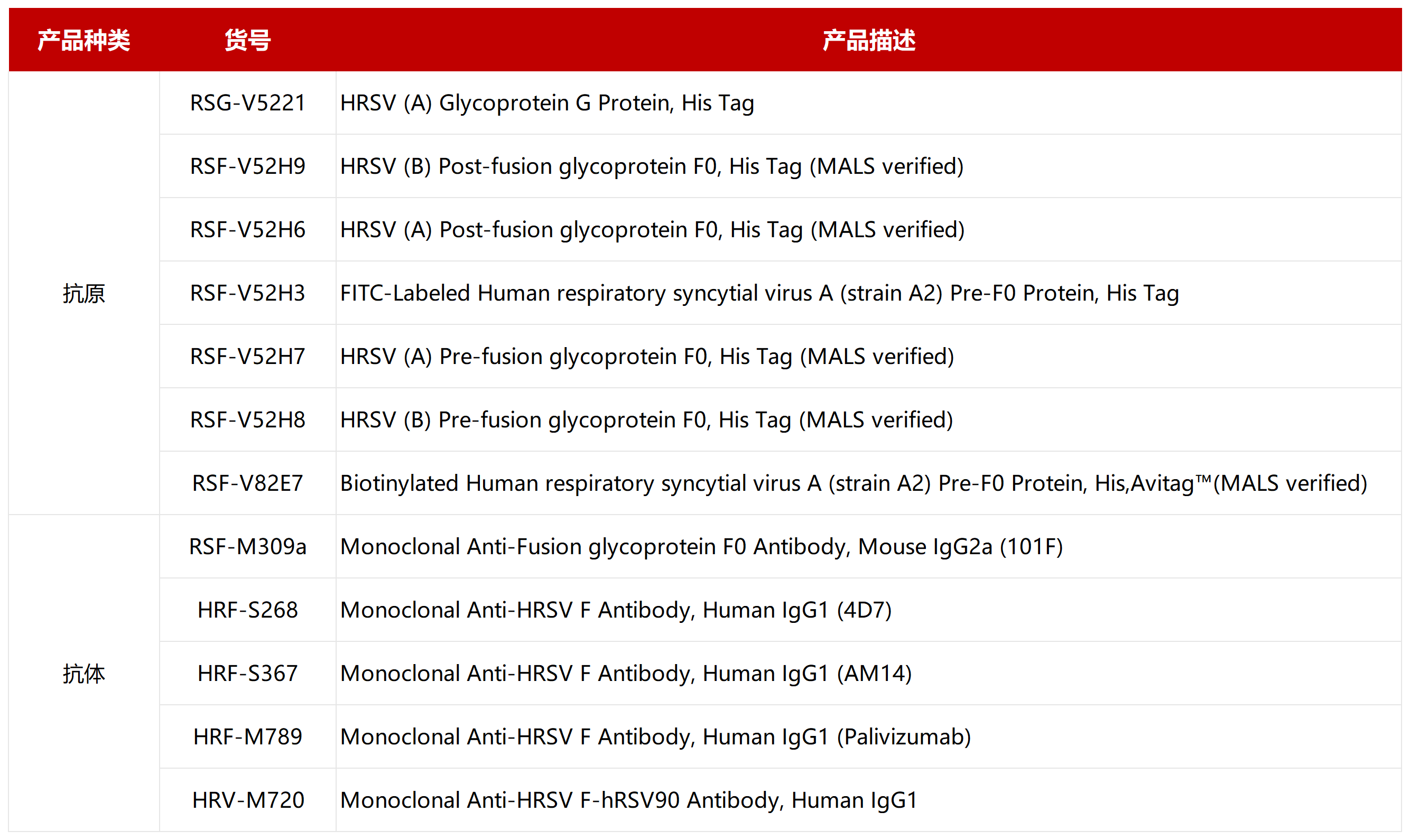
针对RSV疫苗的抗原定量检测,ACROBiosystems百普赛斯开发了一系列抗原定量试剂盒(新品上线,欢迎点击货号查看详情)。
|
产品货号
|
产品描述
|
|
|
HRSV Post-Fusion glycoprotein F0 Specific ELISA Kit
|
|
|
HRSV Pre-Fusion glycoprotein F0 (site Ⅳ) Specific ELISA Kit
|
|
|
HRSV Pre-Fusion glycoprotein F0 (site Ø) Specific ELISA Kit
|
|
|
HRSV Pre-Fusion glycoprotein F0 (site V) Specific ELISA Kit
|
|
|
HRSV Pre-Fusion glycoprotein F0 Specific ELISA Kit
|
|
|
HRSV (A) Pre-Fusion glycoprotein F0 Specific ELISA Kit
|
从临床前疫苗候选物的免疫原性评价到临床研究及上市后研究,免疫原性是疫苗有效性评价时需要关注的重要指标之一。《疫苗临床试验技术指导原则(修订稿)(征求意见稿)》(2024)指出免疫原性的评价指标可通过检测疫苗诱导的适应性免疫水平预测有效性。通过检测血清、全血、黏膜分泌物或其他人体体液等样本中的相关指标可评估体液、细胞、黏膜等免疫应答的强度和持续时间。现阶段临床试验主要采用体液免疫相关指标作为免疫原性评价指标,如中和抗体、IgG 等。
在体液免疫检测时,ELISA是最常用的检测方法。
针对RSV疫苗的体液免疫检测,ACROBiosystems百普赛斯开发了一系列抗体滴度检测试剂盒。
除了抗原定量试剂盒及抗体滴度检测试剂盒外,ACROBiosystems百普赛斯还开发一系列抗原蛋白及特异性抗体,助力RSV疫苗的抗原定量检测及疫苗免疫原性评价。
抗原定量试剂盒
HRSV (A) Pre-Fusion glycoprotein F0 Specific ELISA Kit
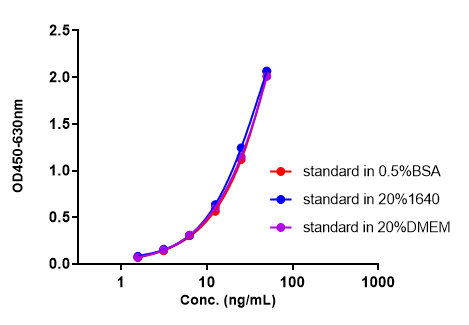
分别测试了不同比例的培养基对标准品干扰,验证0.5%的BSA、20%的1640培养基及 20%的 DMEM培养基对标准品检测的干扰,RSD均符合标准(RSD<15%)。
建议培养基样本的MRD为1:5,小鼠/大鼠血清样本的MRD为1:10。
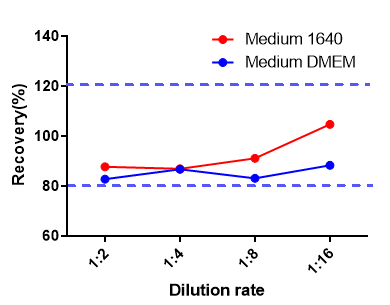
将高浓度的标准品加入到不同的稀释基质中,计算不同稀释比例下的回收率,均在80-120%范围内。
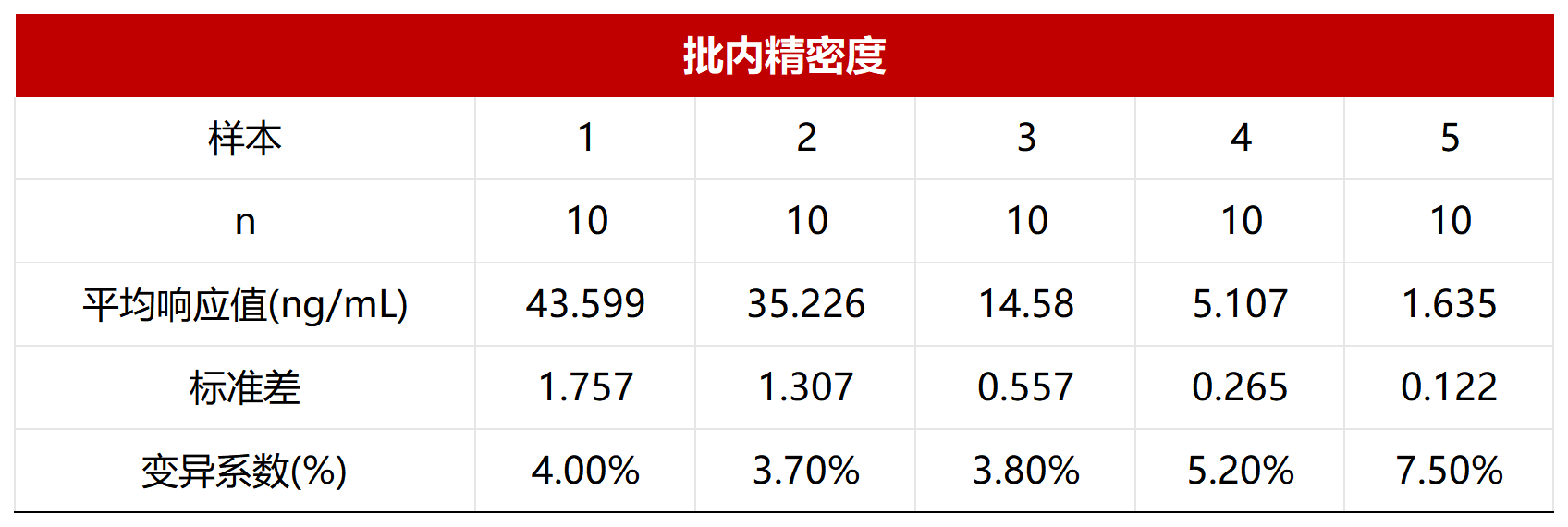
批内精密度:1个分析批,5个已知浓度的样本,每个样本重复测试10次,以评估批内的精密度。
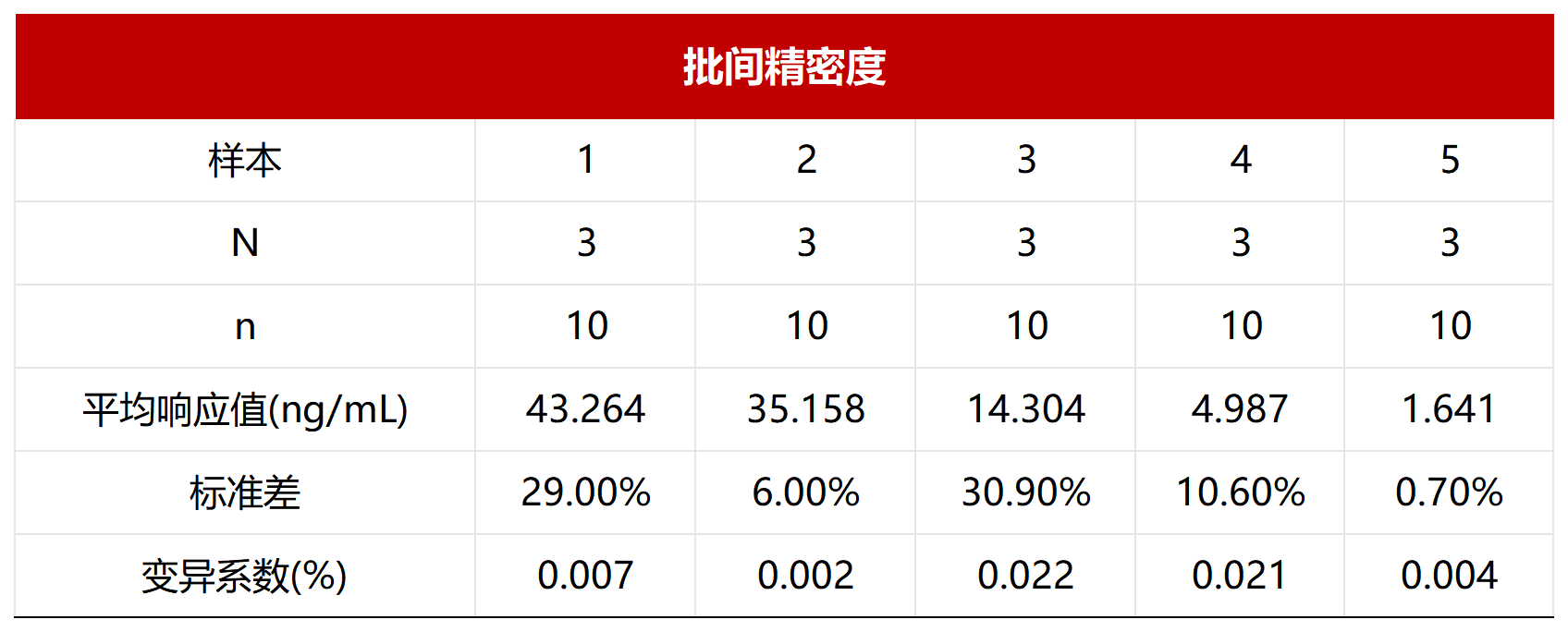
批间精密度:3个分析批,每批5个已知浓度的样本,每个样本重复测试10次,以评估批间的精密度。
*N代表分析批数量,n代表实验重复次数
经验证该项目的批内及批间精密度CV均≤20%,满足试剂盒申明的标准范围。
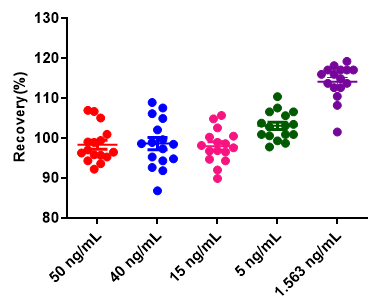
设置5个质控点浓度,每个质控点浓度重复16次,计算回收率均在80-120%范围内。
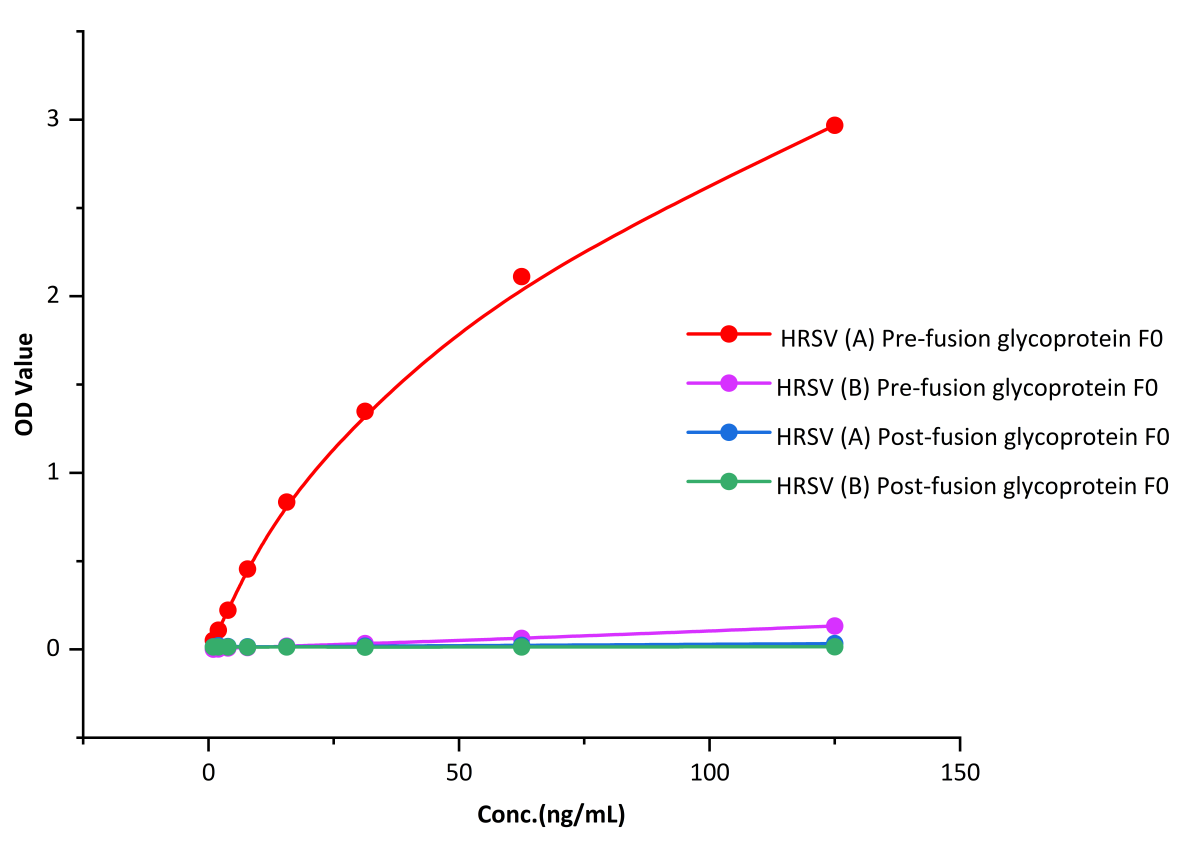
RAS-A200可特异性识别RSV(A) Pre-F蛋白,不识别RSV(B) Pre-F蛋白。
-
下载Application Note,深入了解ACRObiosystems如何识别RSV蛋白构象变化,以确保pre-fusion F0抗原蛋白在结构上的准确,从而帮助您准确进行疫苗评价。
-
-
更多产品推荐
-
-






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining