T细胞衔接器(T Cell Engager, TCE)是一种双特异性抗体,可以同时靶向肿瘤相关细胞表面抗原(Tumor-Associated Antigen,TAA)和T细胞表面受体(T-Cell Receptor,TCR)。与传统单抗相比,TCE双抗的一个显著优势是其强大的专职细胞杀伤能力,通过直接招募激活T细胞,其能够诱导更强烈和更持久的免疫反应。
近年来,国内外多家公司加速推进TCE双抗的商业化,将其视为继ADC之后的新兴增长点。截止2024年12月,全球约有400+条在研的TCE双抗药物管线,且管线数量逐年增加。这其中针对非实体瘤(如多发性骨髓瘤和各类淋巴瘤)及血液病等适应症的管线共计占总管线数的50%以上,且其中约50%管线已经进入临床阶段。除此之外,TCE双抗在针对实体瘤的适应症上也占有约30%的管线数,且近期有所突破。2024年5月,安进宣布其研发的TCE抗体Tarlatamab(商品名称IMDELLTRA)可针对性治疗小细胞肺癌,并且已经获得FDA的加速批准上市。
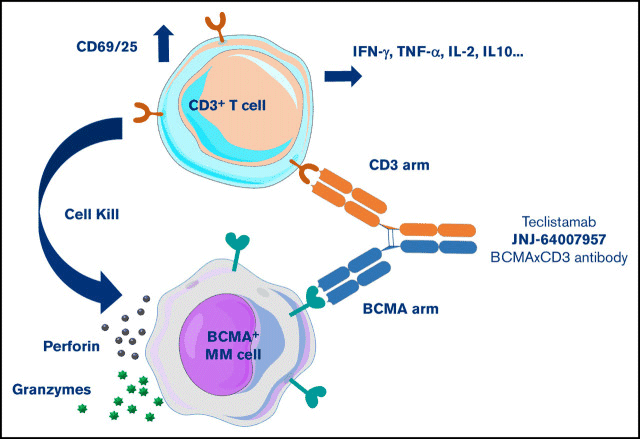
TCE是一种新型抗体,具有独特的Fab端和Fc端结构。其作用机制(Mechanism of Action, MOA)在于一个Fab端结合特定的肿瘤相关抗原(tumor-associated antigen, TAA),另一个Fab端结合T细胞受体(T-cell receptor, TCR),其中CD3是常见的靶点。这种双重靶向使TCE能够精准定位肿瘤细胞,同时将T细胞吸引至肿瘤细胞表面,激活T细胞并诱导肿瘤细胞杀伤。激活后的T细胞通过与肿瘤细胞形成免疫突触裂解肿瘤细胞,同时释放一系列细胞因子(如IFN-γ、TNF-α、IL-2、IL-10等),进一步增强T细胞增殖与抗肿瘤效应(图1)。此外,TCE的Fc端设计可以显著延长其半衰期,降低代谢速度,从而增强药效的持久性。
图1. TCE双抗的作用机制示意图
相比传统的IgG单抗,TCE双抗展现出显著优势。传统IgG单抗主要通过Fc端介导的ADCC、CDC和ADCP机制激活抗原呈递细胞,再由抗原呈递细胞激活T细胞。这一间接机制限制了单抗直接激活T细胞和杀伤肿瘤细胞的能力。而TCE双抗能够直接激活T细胞,显著提高抗肿瘤效果。
更重要的是,TCE的Fab端可以根据不同肿瘤类型的特异性TAA靶点进行定制化设计。例如,针对血液肿瘤的热门靶点包括CD19、CD20、BCMA;而针对实体瘤,常见靶点有DLL3、HER2和CLDN18.2等。
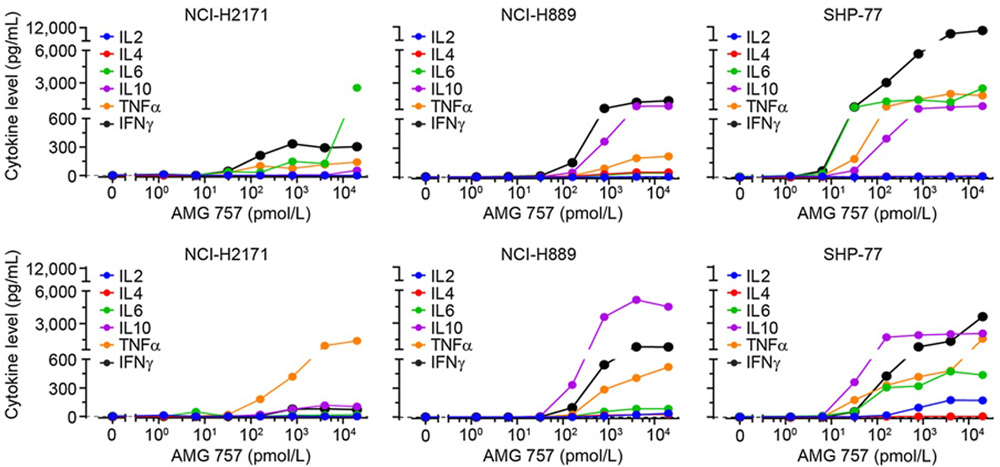
在早期药物开发和临床前阶段,研究人员通过体外培养刺激淋巴细胞分泌细胞因子,分析TCE药物对免疫细胞的刺激作用,从而评价其药效。以在2024年5月上市的靶向CD3和小细胞肺癌特异性抗原DLL3的TCE双抗Tarlatamab为例,其药物作用机制的建立包括了检测不同药物浓度刺激下,细胞上清中的IL-2、IL-4、IL-6、IL-10、IFN-γ和TNF-α细胞因子的分泌情况(图2)。
图2 Tarlatamab体外细胞刺激实验
同时,2014年批准上市的TCE药物Blinatumomab,它是T细胞表面CD3及大B细胞瘤特异性抗原CD19的靶向双抗。根据FDA上公布的临床实验数据,一系列细胞因子(IL-2、IFN-γ、TNF-α、IL-4、IL-6、IL-8、IL-10、IL-12)被确立为临床阶段药效学中T细胞激活的的生物标志物(图3)。
图3. Blinatumomab临床实验中细胞因子标志物检测
综上,在TCE双特异性抗体药物开发过程中,细胞因子作为关键的检测指标,在早期药理药效研究、临床前及临床实验中,通过检测细胞上清/血清中多种细胞因子的分泌量,能充分反应机体免疫系统激活情况。
为了加速TCE药物研发,ACROBiosystems提供多种细胞因子(cytokine)、生物标志物(biomarker)的定量分析ELISA试剂盒。该试剂盒性能经过真实样本和实验的充分验证,保证分析结果的精确性、特异性、准确度、灵敏度和一致性。
-
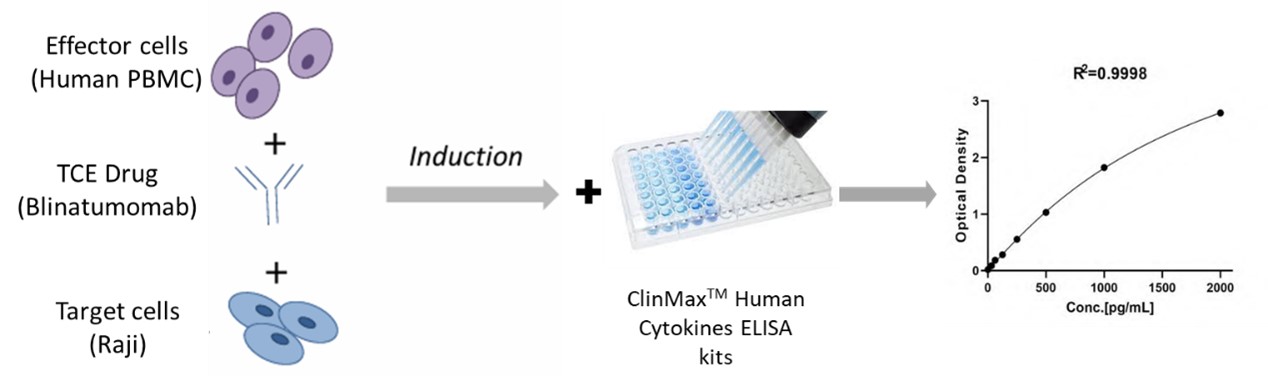
1. 将Human PBMC细胞作为效应细胞,使用GMP ActiveMax® Human T cell Activation/Expansion CD3/CD28 Beads (ACROBiosystems, Cat. No. GMP-MBS001)用于T细胞扩增;
-
2. Day 10用FACS分选CD3+的T细胞与靶细胞(Raji Cells)共同孵育,并用不同浓度的TCE双抗(Blinatumomab)进行刺激;
-
3. TCE双抗同时结合效应细胞上的TCR/CD3和靶细胞上的肿瘤抗原;
-
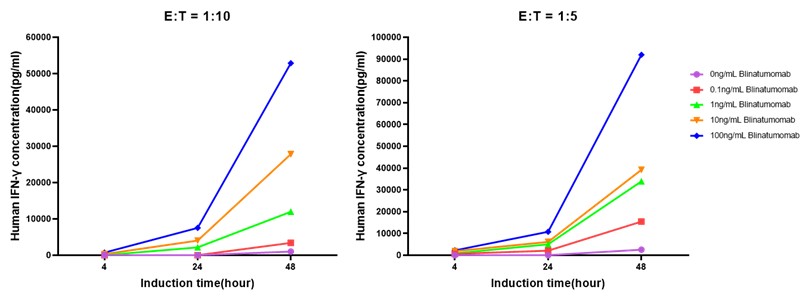
4. TCE双抗的结合刺激IFN-γ,IL-6和IL-10的释放,分别收集0h,24h,48h细胞上清,使用ClinMax™ Human Cytokines ELISA Kit检测上清中细胞因子的含量。
效应细胞和靶细胞在E:T=1:10和1:5比例共培养下,随着药物浓度的增加,100ng/mL Blinatumomab 刺激下,其IFN-γ分泌量都比其他实验组要高(图5)。
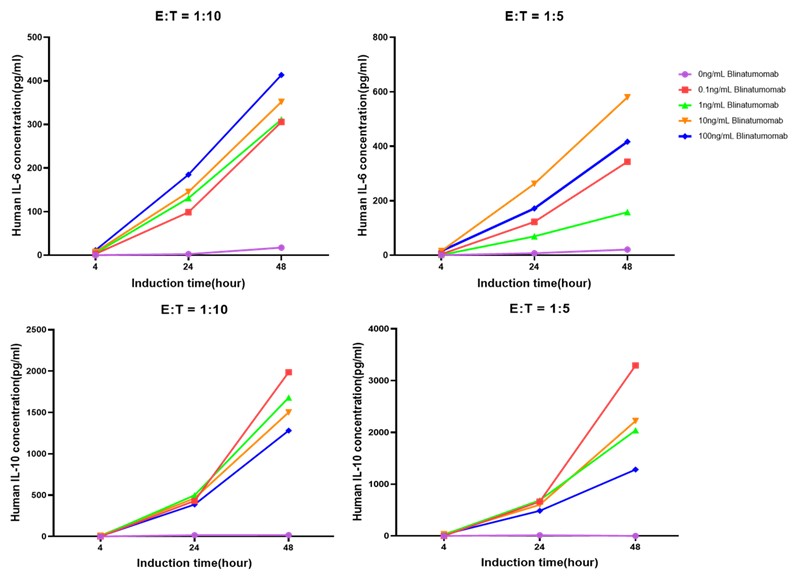
效应细胞和靶细胞在E:T=1:10和1:5比例共培养下,随着药物浓度的增加,IL-6,IL-10的分泌量都比对照组要高(图6)。
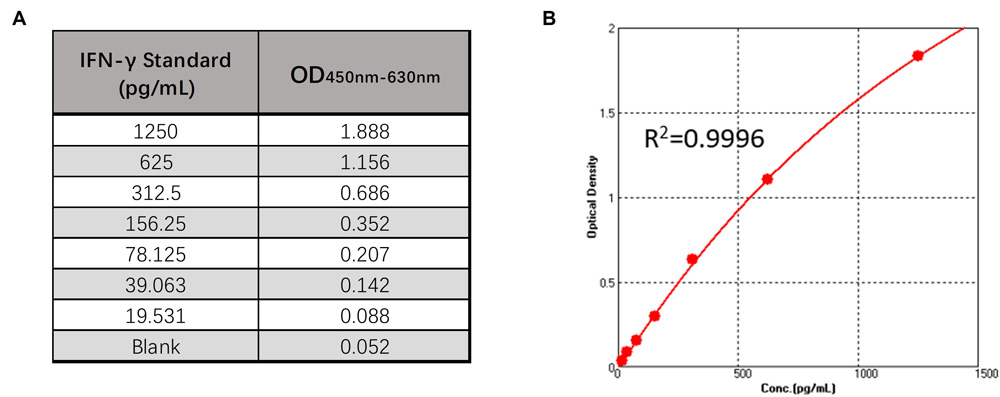
ClinMaxTM人IFN-γ ELISA试剂盒的线性检测范围为19.5 pg/mL – 1250 pg/mL,具体数据见图7。
图7. (A). CRS-A017试剂盒标准品线性检测数据(OD450nm-630nm); (B). CRS-A017试剂盒标准品四参数方程拟合线性图
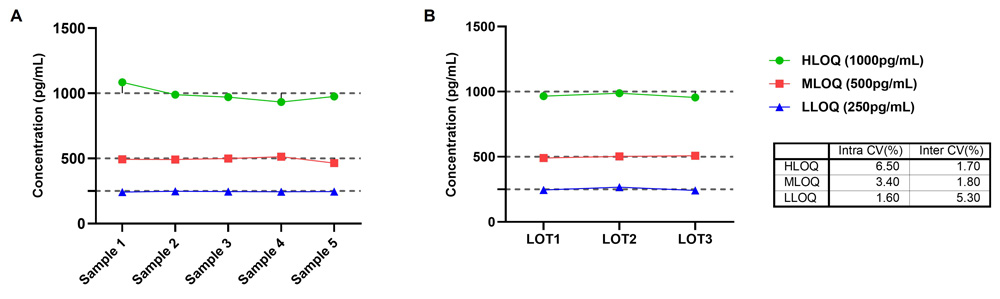
按本产品(CRS-A017)操作说明,测定3个浓度的质控品,每个质控品重复检测10次,计算10次测量结果的平均值(M)、标准差(SD)和变异系数(CV)。结果显示,测定质控品的CV都低于10%,具体结果见图8。
按本产品(CRS-A017)操作说明,测定3个批次3个浓度的QC(pg/mL),每个质控品重复检测3次,计算9次测量结果的平均值(M)、标准差(SD)和变异系数(CV)。结果显示,测定质控品的CV都低于15%,具体结果见图8。
图8. (A). CRS-A017批内精密度数据图;(B). CRS-A017批间精密度数据图及CV值
回收率
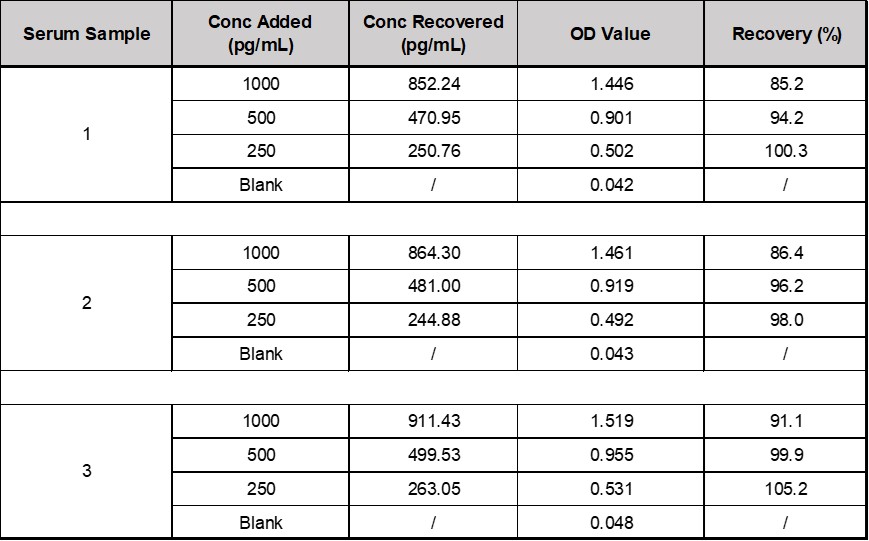
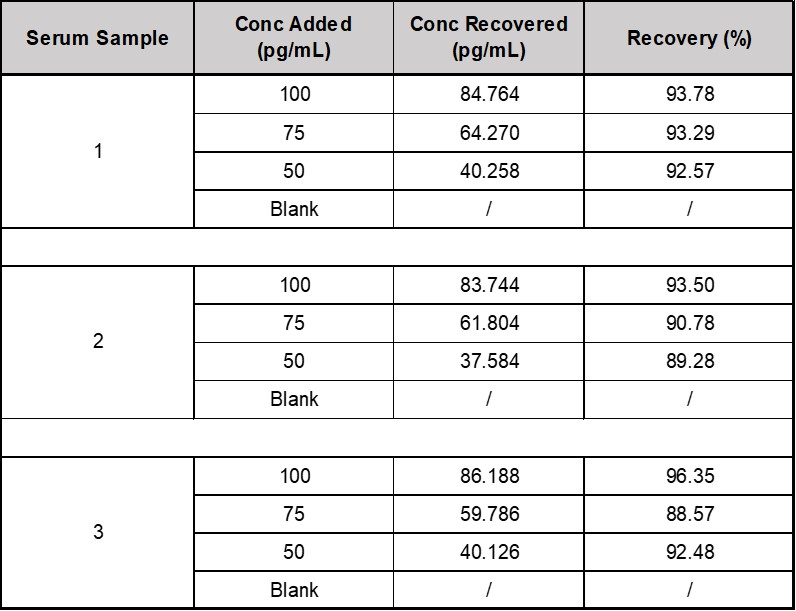
将本产品(CRS-A017)中的参考品,用样本稀释液分别配置成高值血清样本,按照1:19的体积比例加标到血清样本中。按照试剂盒说明书,每个样本均检测2次,求出检测结果的浓度值的平均值。回收率的计算公式=(加标样本值-Blank样本值*0.9)/理论值×100%。本产品回收率都在93.5%的范围内(见下表1)。
表1. CRS-A017回收率数据
稀释线性
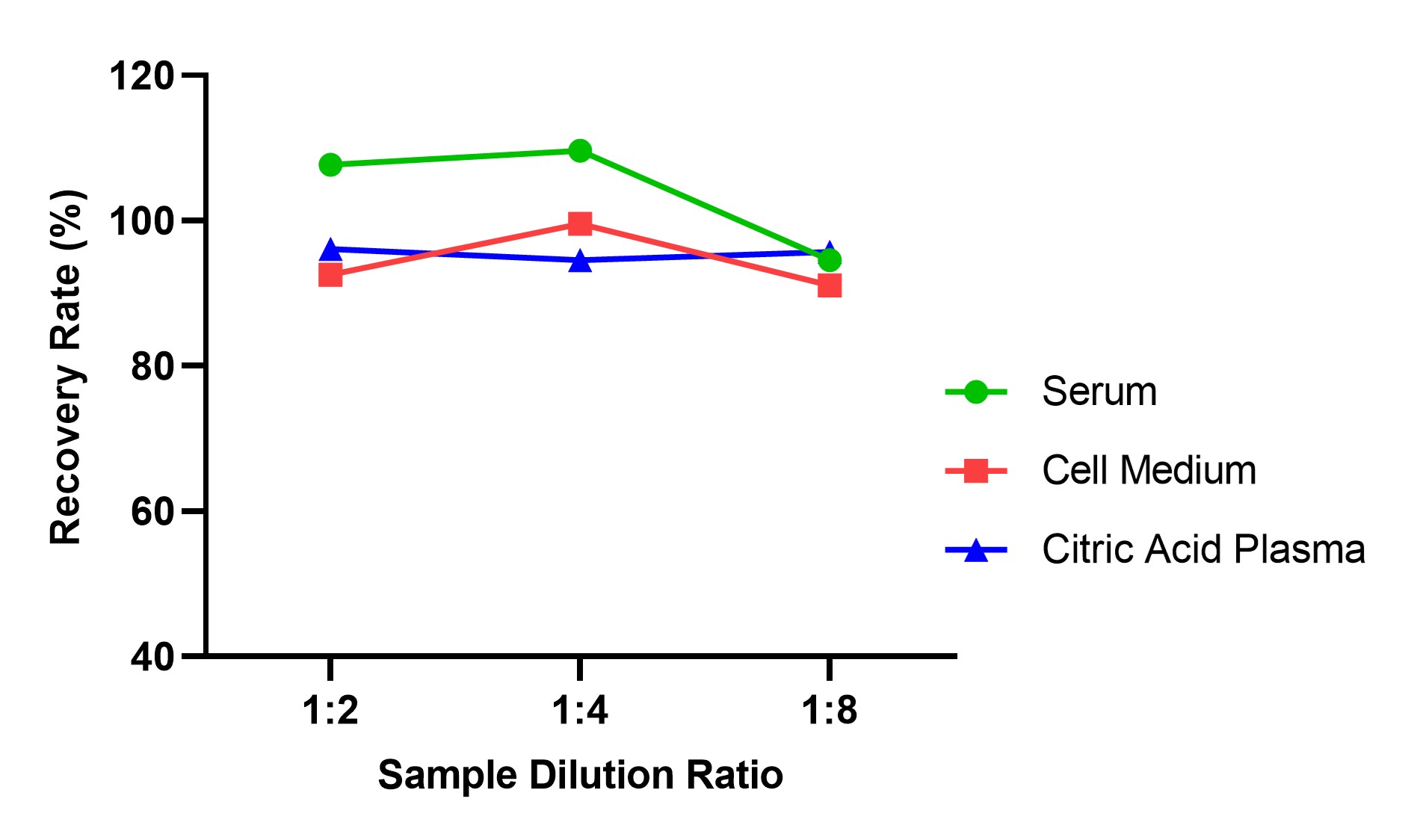
将本产品(CRS-A017)中IFN-γ参考品,用血清样本配置成为高值血清/血浆/细胞上清样本,用样本稀释液依次按1:1进行稀释,每个稀释浓度均检测2次,求检测结果的浓度值的平均值,结果显示,血清/血浆/细胞上清样本各稀释点的检测浓度应都在该待测物浓度标示值的±20%范围内,线性相关系数R2应大于0.95 (见图9)。
图9. CRS-A017稀释线性曲线图
线性范围
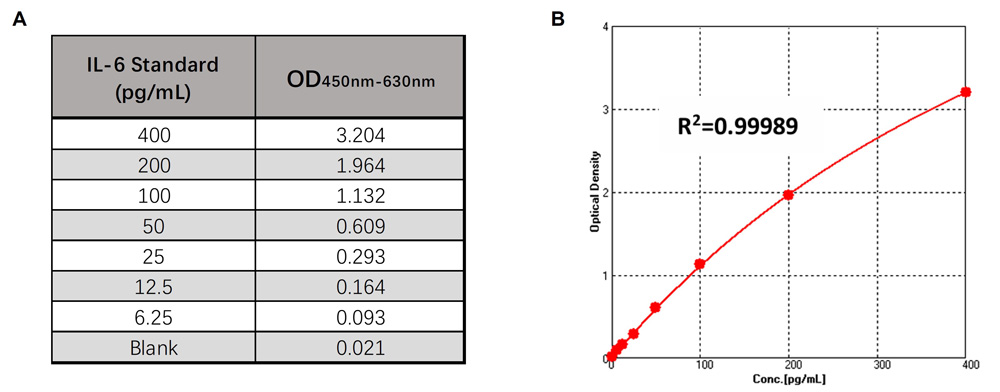
ClinMaxTM人IL-6 ELISA检测试剂盒的线性检测范围为6.25 pg/mL – 400 pg/mL,具体数据见图10。
图10. (A). CRS-B001试剂盒标准品线性检测数据(OD450nm-630nm); (B). CRS-B001试剂盒标准品四参数方程拟合线性图
批内、批间精密度
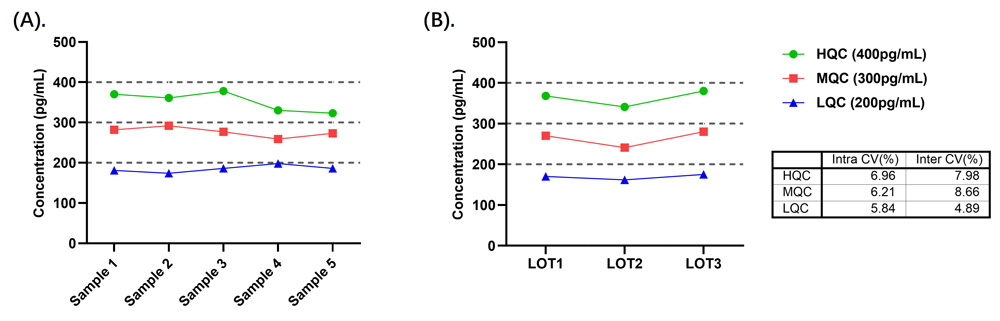
按本产品(CRS-B001)操作说明,测定3个浓度的质控品,每个质控品重复检测10次,计算10次测量结果的平均值(M)、标准差(SD)和变异系数(CV)。结果显示,测定质控品的CV都低于10%,具体结果见图11。
按本产品(CRS-B001)操作说明,测定3个批次3个浓度的QC(pg/mL),每个质控品重复检测3次,计算9次测量结果的平均值(M)、标准差(SD)和变异系数(CV)。结果显示,测定质控品的CV都低于15%,具体结果见图11。
图11. (A). CRS-B001批内精密度数据图;(B). CRS-B001批间精密度数据图及CV值
回收率
将本产品(CRS-B001)中的参考品,用样本稀释液分别配置成高值血清样本,按照1:19的体积比例加标到血清样本中。按照试剂盒说明书,每个样本均检测2次,求出检测结果的浓度值的平均值。回收率的计算公式=(加标样本值-Blank样本值*0.9)/理论值×100%, 本产品回收率平均值为92.29%(见下表2)。
表2. CRS-B001回收率数据






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!






























 膜杰作
膜杰作 Star Staining
Star Staining