【解码帕金森病】从发病机制到精准治疗

帕金森病(Parkinson\'s Disease, PD)是一种常见的神经退行性疾病,随着全球人口老龄化趋势加剧,患病人数持续增长。据统计,目前全球已有超过1000万人受到PD的影响。这种慢性疾病以静止性震颤、动作迟缓、肌肉僵硬和平衡障碍为主要特征,严重影响患者的生活质量。尽管目前的药物治疗可以在一定程度上缓解症状,但仍无法根治。这也促使科研人员不断深入研究其发病机制,积极探索更有效的治疗方法。
多因素交织的病理图谱
PD的核心病理特征是中脑黑质区域多巴胺能神经元(dopaminergic neurons, DNs)的进行性丧失以及路易小体的形成。研究表明,这一病变过程涉及多种分子机制的协同作用。其中,α-突触核蛋白(α-synuclein, α-syn)的异常聚集被认为是关键驱动因素。作为路易小体的主要成分,α-syn可通过类似“朊病毒样”机制在神经元间传播,诱导蛋白质错误折叠和神经元退行性变。
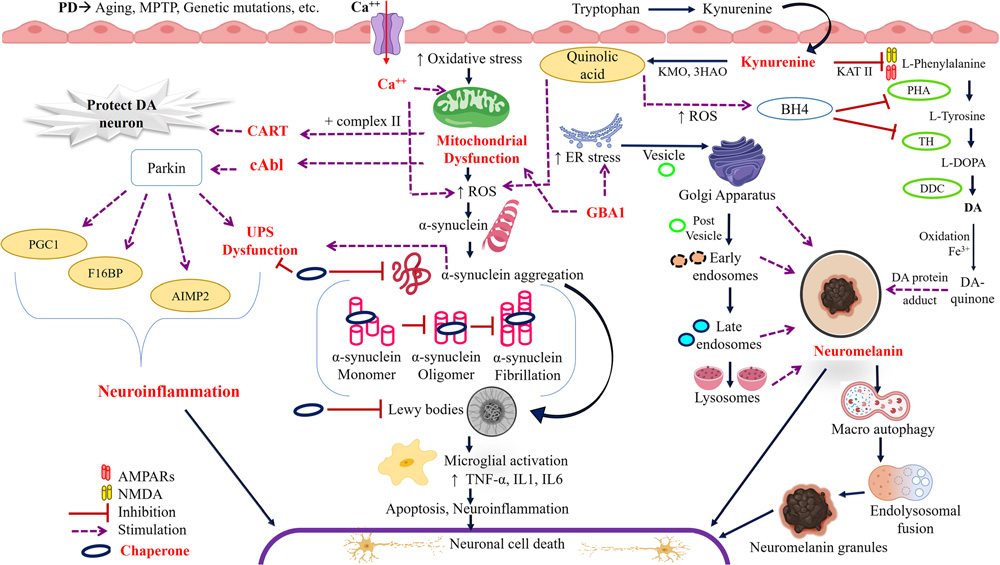
https://doi.org/10.1007/s11011-020-00636-w
PD的复杂调控网络
此外,线粒体功能障碍、溶酶体-自噬通路异常、氧化应激反应及慢性神经炎症等,也被认为PD发病的重要驱动因素。多个信号通路和遗传变异也与上述机制密切相关:如LRRK2(富亮氨酸重复激酶2)突变通过增强其激酶活性,促进α-syn磷酸化并干扰自噬功能;MAO-B(单胺氧化酶B)在催化多巴胺代谢过程中产生过氧化氢等毒性代谢物,从而加剧氧化应激损伤;ADORA2A(腺苷A2A受体)则通过调控纹状体神经元兴奋性及小胶质细胞活化,在神经炎症与运动功能调控中发挥关键作用。
从细胞到脑类器官
在PD的发病机制研究和新药开发过程中,构建可靠的疾病模型至关重要。传统的MPTP或6-OHDA动物模型虽可在一定程度上再现DNs的退变,但其在反映人类复杂的遗传背景方面仍存在显著的局限性。
近年来,随着诱导多能干细胞(induced pluripotent stem cells, iPSCs)技术的迅速发展,研究人员能够从不同来源的体细胞中重编程获得DNs。这些细胞模型不仅有助于揭示疾病相关的细胞表型与功能差异,还为药物筛选、机制研究以及个体化治疗策略的开发提供了理想的平台。
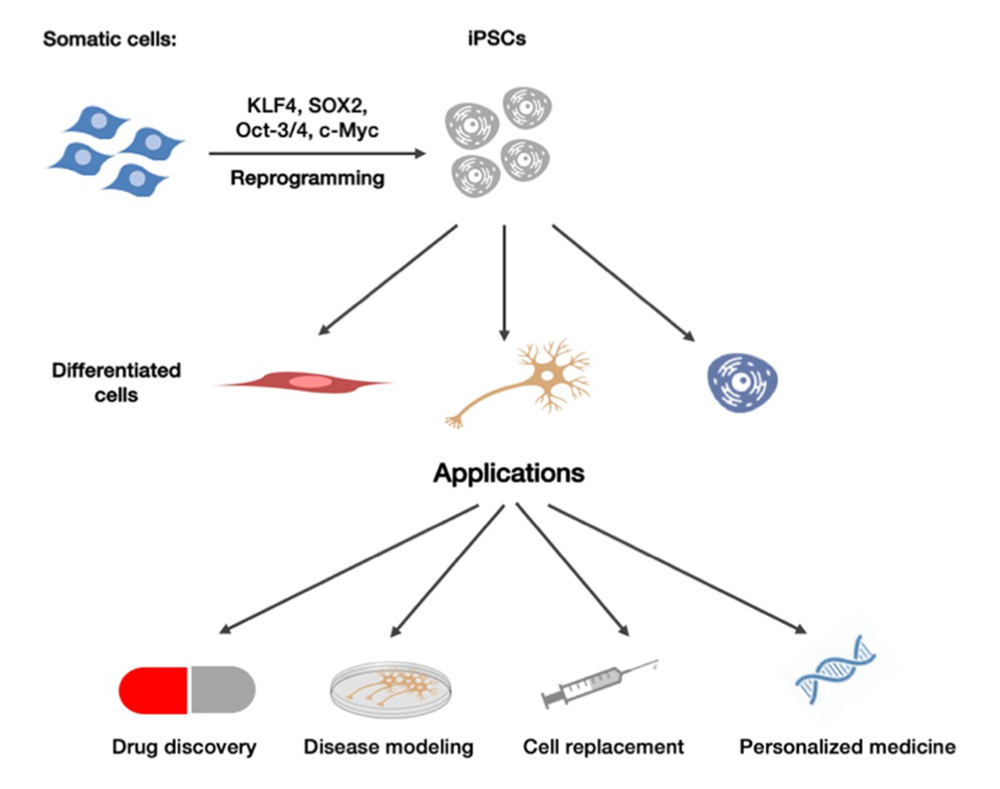
https://doi.org/10.3390/ijms19123972
iPSCs的潜在应用
在此基础上,脑类器官作为由多种神经细胞组成的三维结构,进一步提升了模型的生理相关性,能够更真实地模拟α-syn聚集、神经炎症和神经元退行性变等关键病理过程。例如,使用ACROBiosystems百普赛斯的脑类器官分化试剂盒(货号 RIPO-BWM001K)分化得到的脑类器官(货号 CIPO-BWL001K),与不同浓度的α-syn预制前体纤维(Pre-formed Fibrils, PFFs)共同孵育,可构建PD模型。实验结果显示,PFFs处理后脑类器官中MAP2和TH表达水平下降,表明成熟神经元(MAP2)和DNs(TH)受到了α-syn诱导的毒性损伤,验证了该模型在病理机制研究和药物筛选中的潜力。
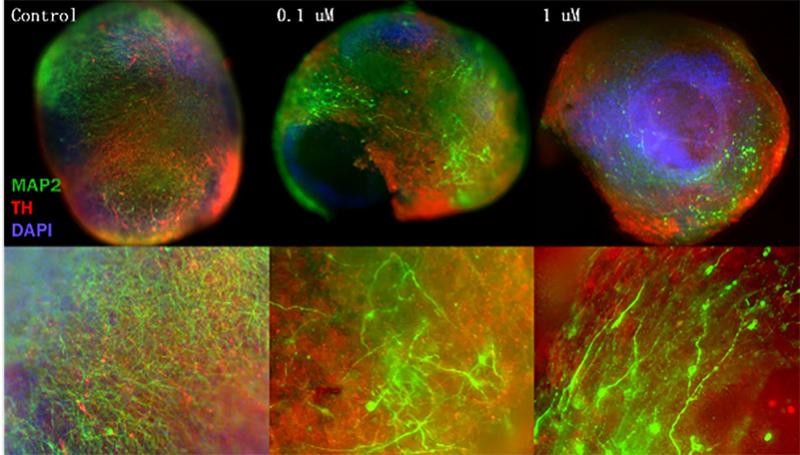
α-syn PFFs诱导脑类器官中的神经元损伤
2025年4月10日,美国食品药品监督管理局(FDA)宣布将逐步取消对单克隆抗体等药物的动物实验强制要求,鼓励使用包括脑类器官在内的替代技术,进一步推动了脑类器官模型在PD研究中的应用潜力。

从对症缓解迈向精准治疗
目前,PD的标准治疗仍以多巴胺替代疗法为核心,如左旋多巴和多巴胺受体激动剂,虽能显著缓解运动症状,但难以延缓疾病进展,且长期使用可能引发“开关现象”或异动症等并发症。近年来,治疗策略正逐步从对症缓解迈向基于病理机制的精准治疗。例如,靶向α-syn聚集的单克隆抗体旨在阻断其异常传播;针对LRRK2突变的小分子抑制剂则通过调节致病信号通路和细胞自噬发挥作用;ADORA2A受体拮抗剂则影响神经元兴奋性及神经炎症,拓展了非多巴胺通路的治疗思路。此外,iPSCs来源的DNs或脑类器官构建的药物筛选平台,也为个体化精准治疗提供了有力支持。
助力PD研究更进一步
ACROBiosystems百普赛斯可提供针对PD研究的前沿解决方案,包括靶点蛋白、预制前体纤维(Pre-formed Fibrils, PFFs)、多巴胺能神经元以及脑类器官,助力加速PD的基础与临床研究。



-
α-syn高纯度经SDS-PAGE及SEC-MALS双重验证
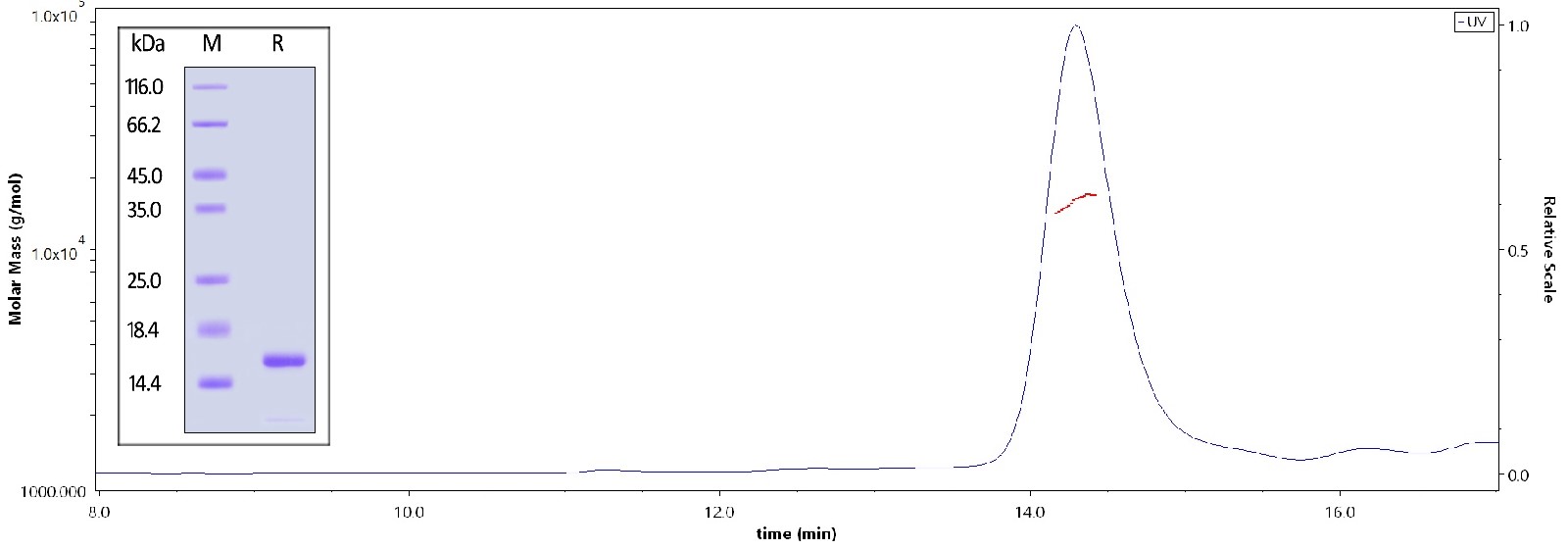
Human Alpha-Synuclein, Tag Free (Cat. No. ALN-H5214) on SDS-PAGE under reducing (R) condition. The purity of the protein is greater than 90%. As verified by SEC-MALS, the purity is more than 90% and the molecular weight of this protein is around 13-19 kDa.
-
α-syn PFFs聚集形态经电镜观测确认

Transmission electron microscopy (TEM) of alpha-synuclein preformed fibrils (Cat. No. ALN-H51H4). Fibril structure is visible on negative stain TEM images of ALN-H51H4 (Routinely tested).
-
多巴胺能神经元自发放电活性经微电极阵列(MEA)检测验证
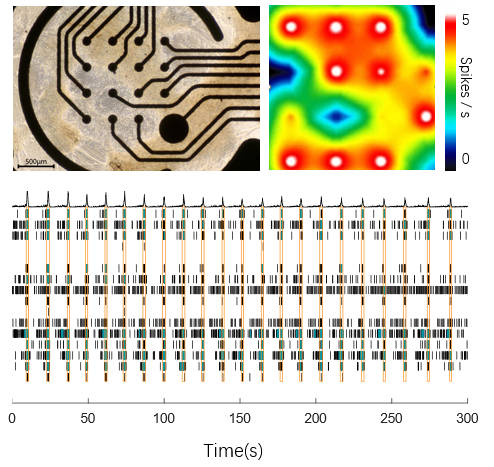
Human iPSC-Derived Dopamine Neurons (Cat. No. CIPC-DDC001) cultured on MEA plates show strong spontaneous firing with regular burst patterns, confirming successful network formation and functional connectivity, suitable for neurophysiological research.
-
中脑类器官多标志物表达经免疫荧光验证
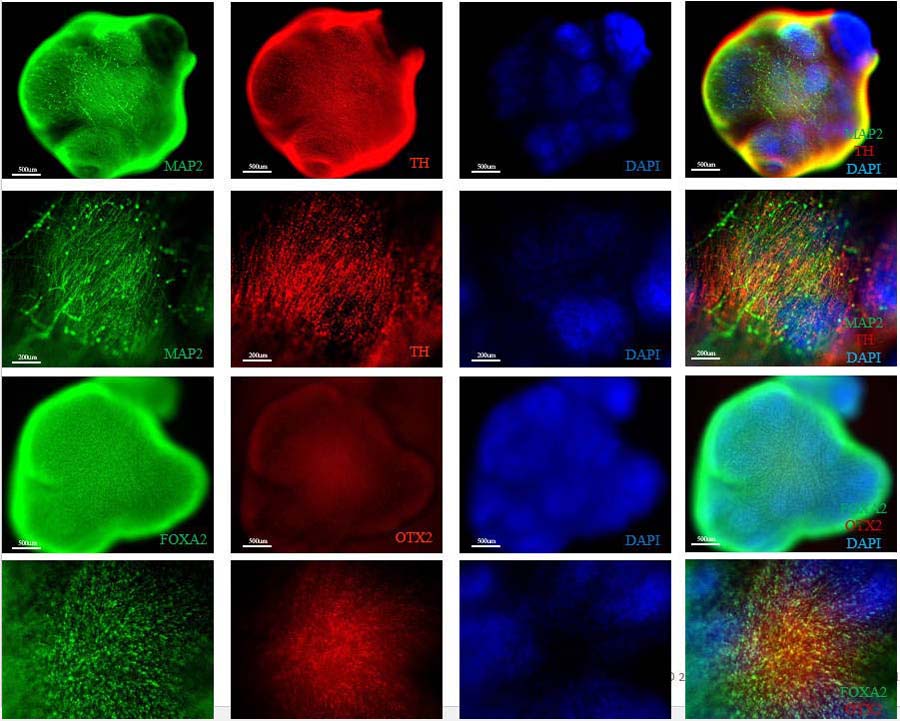
The midbrain organoids (Cat. No. CIPO-MBWL001K) exhibit high expression of TH (dopaminergic neurons), MAP2 (mature neurons), as well as FOXA2 and OTX2 (dopaminergic progenitor cells) on day 37.
点击图片,查看Aneuro助力脑科学研究
点击图片,查看Organoid Toolbox类器官解决方案
点击图片,参与“下单类器官送徽章”活动
参考文献
1. Pingale T, Gupta G L. Current and emerging therapeutic targets for Parkinson’s disease[J]. Metabolic Brain Disease, 2021, 36: 13-27. https://doi.org/10.1007/s11011-020-00636-w
2. Bordoni M, Rey F, Fantini V, et al. From neuronal differentiation of iPSCs to 3D neuro-organoids: Modelling and therapy of neurodegenerative diseases[J]. International Journal of Molecular Sciences, 2018, 19(12): 3972. https://doi.org/10.3390/ijms19123972



























